Aktualisierte Stellungnahme von DGPM, DGGG, DGPGM, DGPI, GNPI und NSK zu SARS-CoV-2/COVID-19 und Schwangerschaft, Geburt und Wochenbett (Stand 02.10.2020)
Das vorliegende Update versteht sich als Fortschreibung der bereits publizierten Empfehlungen der deutschen geburtshilflichen und pädiatrischen Fachgesellschaften zur Versorgung infizierter Schwangerer und deren Neugeborenen (1-4).
Als Neuerung werden in zwei Teilen
- PRAKTISCHE EMPFEHLUNGEN mit jeweiliger kurzer Erläuterung sowie
- HINTERGRUNDINFORMATIONEN als Review des aktuellen Wissenstandes über SARS-CoV-2/COVID-19 in Schwangerschaft, Geburt und Wochenbett dargestellt.
Das Update nimmt Stellung zu den Kernfragen der prä-, peri- und postnatalen Betreuung bei SARS-CoV-2 und COVID-19, auf Grundlage der bis zum 01.10.2020 verfügbaren Publikationen sowie der CRONOS-Registerdaten bis zum 02.10.2020, und wird im Konsens der nachfolgenden Fachgesellschaften getragen:
- Deutsche Gesellschaft für Perinatale Medizin (DGPM)
- Deutsche Gesellschaft für Gynäkologie und Geburtshilfe (DGGG)
- Deutsche Gesellschaft für Pränatal- und Geburtsmedizin (DGPGM)
- Deutsche Gesellschaft für Pädiatrische Infektiologie (DGPI)
- Gesellschaft für Neonatologie und Pädiatrische Intensivmedizin (GNPI)
- Nationale Stillkommission (NSK)
Die Stellungnahmen basieren auf einem sorgfältig abgestimmten Expert*Innenkonsens und können sich – insofern neue Erkenntnisse veröffentlicht werden – zeitnah ändern. Die Verantwortung für das konkrete Vorgehen bleibt bei dem vor Ort medizinisch betreuenden Team, dessen Entscheidungen durch diese Empfehlung unterstützt werden sollen.
PRAKTISCHE EMPFEHLUNGEN
1. Schwangere sollen bei Vorstellung in der Praxis und Klinik Mund und Nase bedecken. Das Tragen eines Mund-Nasen-Schutzes während der Geburt muss im Einzelfall geprüft werden.
Das Bedecken von Mund und Nase ist bei Betreten der Entbindungsklinik empfohlen (5, 6). Dies gilt sowohl für Schwangere als auch für mögliche Begleitpersonen.
Bei unklarem SARS-CoV-2 Status ist unter Geburt das Tragen eines Mund-Nasen-Schutzes (MNS) durch die Patientin zu diskutieren, bei positivem Status zu empfehlen, um das geburtshilfliche Personal v.a. in der aktiven Austreibungsperiode zu schützen. Dabei soll der Oxygenierungsstatus der Mutter und deren subjektives Wohlbefinden berücksichtigt werden (7).
Für das betreuende Personal ist das Tragen eines Mund-Nasen-Schutzes unabhängig vom SARS-CoV-2 Status während der Pandemie bei jeder Entbindung empfohlen (6). Bei positivem SARS-CoV-2 Status der Gebärenden muss das geburtshilfliche und pädiatrische Personal in der für den Umgang mit SARS-CoV-2 Patienten empfohlenen persönlichen Schutzausrüstung agieren (1, 2, 7-9).
2. Bei SARS-CoV-2 positiven Schwangeren werden ultrasonographische Verlaufskontrollen (Biometrie, Doppler, Fruchtwassermenge) in 2- bis 4-wöchentlichen Abständen empfohlen.
Die Ultraschalldiagnostik ist elementarer Bestandteil der Schwangerenvorsorge. Notwendige Untersuchungen erfolgen unabhängig einer SARS-CoV-2 Infektion entsprechend der Mutterschaftsrichtlinien. Eine häusliche Quarantäne darf hier nicht zu einer Versorgung unterhalb des Standards führen. Liegt der Infektionszeitpunkt in der frühen Schwangerschaft, sollte großzügig auch ein Ersttrimester-Screening beziehungsweise eine erweiterte Feindiagnostik angeboten werden (10, 11).
Bei SARS-CoV-2 positiven Schwangeren werden serielle Wachstums- und Dopplerkontrollen in maximal 4-wöchentlichen Abständen empfohlen, da histopathologische Hinweise für eine Plazentainsuffizienz (s.u.) gefunden wurden (12).
3. Die Applikation antenataler Steroide und Tokolytika bei drohender Frühgeburt soll indikationsgerecht erfolgen.
Eine fetale antenatale Steroidgabe erfolgt unabhängig von SARS-CoV-2 nach geburtshilflichen Kriterien bis 34+0 SSW mit Betamethason bzw. Dexamethason (13). Es gibt keine Hinweise auf zusätzliche Nebenwirkungen bei Applikation nach SARS-CoV-2 Infektion/COVID-19 (14). Nichtsteroidale Antirheumatika, wie ASS oder Indomethacin können weiterhin in den Indikationen zur Präeklampsie-Prävention oder Wehenhemmung verwendet werden (15). Kardiopulmonal wirksame Medikamente wie Fenoterol sollten aufgrund ihres Nebenwirkungsprofils (16) restriktiv eingesetzt werden. Andere geburtshilflich typische Medikamente sind nach aktuellem Kenntnisstand ohne Beschränkungen anwendbar (17).
4. Eine Thrombembolieprophylaxe mit niedermolekularem Heparin soll risikoadaptiert angewendet werden. Bei stationärer Behandlung ist eine Therapie angezeigt.
Es besteht auch in der Schwangerschaft ein erhöhtes Risiko für thrombembolische Ereignisse bei SARS-CoV-2 Infektion und COVID-19 Erkrankung (13, 17-19).
Bei Verdacht auf oder Nachweis einer SARS-CoV-2 Infektion in der Schwangerschaft muss eine (Neu-)Bewertung individueller thrombembolischer Risiken erfolgen – hierbei soll unter anderem eine quarantänebedingte Mobilitätseinschränkung berücksichtigt werden (20). Empfehlungen für die Isolation zu Hause sollten gegeben werden (Hydratation, Mobilisierung, ggf. Kompressionstherapie) (21). Eine Sensibilisierung für thrombosetypische Symptome ist sinnvoll.
Alle Schwangeren mit vermuteter oder bestätigter COVID-19 Erkrankung sollen bei Hospitalisierung eine medikamentöse Thrombembolieprophylaxe mit niedermolekularem Heparin erhalten (20, 22). Ausnahmen bestehen, wenn in absehbarer Zeit (12h) die Entbindung bevorsteht oder relative Kontraindikationen (z.B. gerinnungsrelevante Laborveränderungen, aktive Blutung, etc.) vorliegen (23). Eine verlängerte PT und aPTT sollten hierbei nicht als Kontraindikation für die Thromboseprophylaxe betrachtet werden (21). Vorbestehende Antikoagulationstherapien werden fortgesetzt.
Der Einsatz erweiterter mechanischer Kompressionstherapie (z.B. intermittierende pneumatische Wadenkompression) sollte erwogen werden, wenn die Thromboseprophylaxe z.B. aufgrund einer Thrombozytopenie pausiert wird (21).
Eine medikamentöse Thrombembolieprophylaxe sollte für mindestens 10 Tage nach Entlassung fortgeführt werden (20). Dies gilt auch, wenn eine stationäre Behandlung im Wochenbett begonnen wird. Hier ist ein Applikationszeitraum von bis zu 6 Wochen post partum zu überlegen (24, 25). Eine bereits begonnene Thrombembolieprophylaxe sollte postpartal fortgeführt werden (25).
Es existieren derzeit mehrere, allenfalls in Details gering voneinander abweichende, Empfehlungen zur thrombembolischen Prophylaxe schwangerer Frauen mit vermuteter oder bestätigter SARS-CoV-2 Infektion. In Tabelle 1 sind die bestehenden Empfehlungen in Abhängigkeit der individuellen Betreuungssituation unter Berücksichtigung spezifischer Risikofaktoren zusammengefasst.
Tabelle 1: Empfehlungen zur thrombembolischen Prophylaxe bei Schwangereren mit vermuteter oder bestätigter SARS-CoV-2 Infektion/COVID-19 Erkrankung (19, 26). VTE: venöse Thrombembolie, NMH: Niedermolekulares Heparin
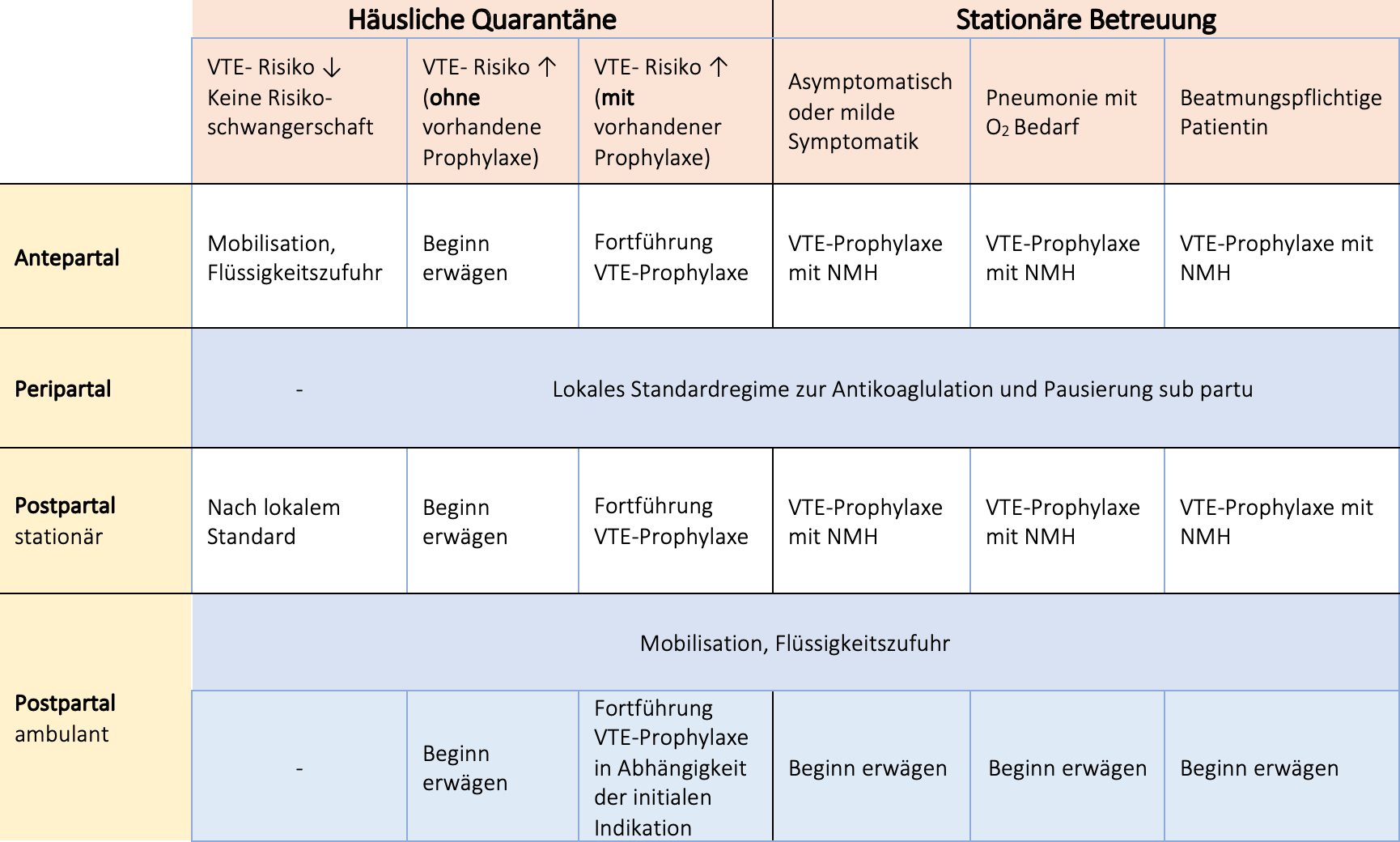
5. Weder eine SARS-CoV-2 Infektion noch die COVID-19 Erkrankung allein stellen eine Entbindungsindikation dar. Eine relevante mütterliche respiratorische Beeinträchtigung kann eine Entbindung erforderlich machen.
In Terminnähe kann der physiologische Verlauf und Entbindungszeitpunkt abgewartet werden. Besteht aus geburtshilflicher Sicht eine Entbindungsindikation bei einer SARS-CoV-2 positiven Schwangeren, sollte eine Geburtseinleitung oder Schnittentbindung nicht verschoben werden (1, 5, 17). Soweit geburtshilflich vertretbar, sollten bei der Festlegung des Entbindungszeitpunktes infektiologische Gesichtspunkte (Abwarten bis negative PCR, klinischer Verlauf) berücksichtigt werden. Für die kritisch kranke geburtshilfliche Patientin mit COVID-19 sollte eine Abwägung des klinischen Bildes und geburtshilflicher Aspekte zwischen supportiver COVID-19 Therapie mit Prolongation der Schwangerschaft und der Entbindung erfolgen (27).
6. Die vaginale Entbindung wird bei SARS-CoV-2 Infektion oder COVID-19 Erkrankung empfohlen.
Die Wahl des Entbindungsmodus sollte geburtshilflichen Kriterien folgen (1, 5, 17). Die bislang überdurchschnittlich hohe Rate an Kaiserschnittentbindungen (40 – 96 %) gerade in der Anfangszeit des COVID-19 Ausbruchs sind vermutlich eher der zunächst herrschenden Unsicherheit in Bezug auf die Erkrankung und lokalen Gegebenheiten geschuldet (28, 29). Ein aktuelles Review asiatischer Studien (30) beschreibt eine gepoolte Sectiorate von 88 % (95 % KI: 82,0 % – 94,0 %). Lokale Unterschiede in der Sectiohäufigkeit bei COVID-19 finden sich auch in den USA (ca. 40 %) und Europa (38 %) (31). Die aktuellste Auswertung (Stand 08.06.2020) der britischen UKOSS-Registerdaten zeigt eine Sectiorate von 60 % bei Schwangeren mit SARS-CoV-2 Infektion, wobei hiervon ca. 50 % aus mütterlicher oder fetaler Beeinträchtigung resultierte. 20% der Kaiserschnitte erforderten eine Allgemeinanästhesie (aufgrund der Schwere der COVID-19 Symotomatik bzw. der Dringlichkeit der Entbindung) (32). Eine aktuelle schwedische Fallserien (n = 67) berichtet dagegen von nur 30 % Sectiones (33). Das deutsche CRONOS Register berichtet zum 02.10.2020 auf der Basis von 247 registrierten Patientinnen eine Rate von 40,5 % Sectiones (34). Die Empfehlung zur vaginalen Entbindung bei SARS-CoV-2 Infektion ist internationaler Konsens (5, 35). Ist der Spontanpartus angestrebt, so ist im Kreißsaal ein kontinuierliches CTG-Monitoring und eine Überwachung der mütterlichen Vitalparameter mit SpO2 obligat (36, 37). Es ist auf eine ausgeglichene Flüssigkeitsbilanz zu achten, da eine Positivbilanzierung zu Lungenödemen und einer Verschlechterung der maternalen Oxygenierung führen kann (25).
Eine Amniotomie und die Überwachung der fetalen Herzfrequenz mittels Kopfschwartenelektrode können bei entsprechender Indikation erfolgen. Kontakt zu Stuhl, in dem nachweislich Virus enthalten sein kann, sollte vermieden werden (38, 39). Daher ist von einer Wassergeburt abzuraten.
7. Ein Screening auf SARS-CoV-2 aus geeignetem respiratorischen Material (z.B. tiefer Nasopharynxabstrich, Rachenspülwasser) bei stationärer Aufnahme oder Aufnahme zur Geburt kann zum Schutz des Personals sinnvoll sein.
Es gibt keinen internationalen Konsens für ein generalisiertes Screening aller Schwangerer zum Virusnachweis bzw. Infektionsausschluss (5). Jede Patientin sollte jedoch während der Pandemie bei Aufnahme nach Symptomen und Anamnese auf SARS-CoV-2 Infektionsrisiken befragt werden. Der Anteil asymptomatischer inifizierter Schwangerer liegt bei bis zu 89 % (40, 41). Das Gefährdungspotential für das medizinische Personal ist hoch.
Analog den Empfehlungen der Deutschen Gesellschaft für Allgemein- und Visceralchirurgie (42) sollte unter Berücksichtigung der jeweiligen epidemiologischen Lage eine SARS-CoV-2 Testung vor elektiven Eingriffen, wie z.B. einer geplanten Kaiserschnittentbindung, Cerclage oder Geburtseinleitung erfolgen. Das Resultat soll vor Aufnahme vorliegen.
8. Die Anwesenheit einer gesunden Begleitperson unter der Geburt ist möglich und sinnvoll.
Bereits in der ersten deutschen Empfehlung vom März 2020 wird die Begleitung der Kreißenden durch eine Vertrauensperson unterstützt (1, 3, 43).
Entsprechend der lokalen Infektionssituation sollen individuelle Regelungen getroffen werden (z.B. Begrenzung auf eine Person, Tragen eines MNS, unauffällige Anamnese, kein Fieber, kein Verlassen des Gebärraumes durch die Begleitperson, kein positiver Virusnachweis oder 2 negative Testergebnisse nach stattgehabter Infektion).
9. Eine SARS-CoV-2 Infektion bzw. COVID-19 Erkrankung stellt keine Kontraindikation zur Regionalanästhesie (PDA/SpA) dar und sollte zu einem frühen Zeitpunkt in Erwägung gezogen werden. Der Einsatz von Lachgas (N2O) sub partu wird aufgrund möglicher Aerosolbildung kontrovers diskutiert.
Eine frühe suffiziente Schmerzlinderung kann die kardiopulmonale Belastung sub partu reduzieren. Der Analgetikaeinsatz von Substanzen mit atemdepressivem Nebenwirkungsprofil sollte in Abwägung des mütterlichen Status erfolgen (25, 36). Eine SARS-CoV-2 Infektion bzw. COVID-19 Erkrankung stellt keine Kontraindikation zur Regionalanästhesie (Periduralkatheter/Spinalanästhesie) dar (44, 45). Eine frühzeitige neuraxiale Analgesie der Wehen wird weiterhin empfohlen, um die Verfügbarkeit im Falle einer sekundären Schnittentbindung sicherzustellen, andernfalls sollte hierfür möglichst eine Spinalanästhesie durchgeführt werden, um die erhöhte aerosolbedingte Infektionsgefahr im Rahmen der Intubationsnarkose für das Personal zu vermeiden. Falls dies jedoch notwendig oder unvermeidlich (Notsectio) ist, sollte die Vollnarkose den allgemeinen Empfehlungen für die Intubation und Extubation bei SARS-CoV-2 infizierten Patienten folgen (46, 47).
Die „Society of Obstetric Abesthesia and Perinatology“ schlägt vor, von einer Analgesie mit Lachgas abzusehen, da unzureichende Daten zur Reinigung, Filterung und potenziellen Aerosolbildung der verwendeten Systeme bestehen (48). Während deutsche Empfehlungen die Nutzung von Lachgas zur peripartalen Analgesie ebenfalls ablehnend gegenüberstehen, sieht das Royal College of Obstetrics and Gynecology hierfür keine Kontraindikation (26), wenn ein personenbezogener mikrobiologischer Filter und eine Einmalmaske verwendet werden (1, 36).
10. Die Anzahl betreuender Personen von SARS-CoV-2 positiv Gebärenden sollte auf ein Mindestmaß begrenzt werden. Das neonatologische und anästhesiologische Team sollte frühzeitig und kontinuierlich informiert werden.
Gebärende mit vermuteter oder gesicherter SARS-CoV-2 Infektion sollten unter geeigneten Infektionsschutzmaßnahmen zur Entbindung vorgestellt und aufgenommen werden (49). Die hierfür erforderliche Logistik und klare Zuständigkeiten müssen prospektiv etabliert werden. Hierzu gehören neben der klaren Benennung der zuständigen Personen, die Festlegung möglicher Isolationsräume (wenn möglich Anpassung der Raumlufttechnik hin zu Unterdruck, wenn möglich auch im OP), die Simulation COVID-spezifischer Szenarien im Team aller beteiligter Professionen, das Training des Gebrauchs von Schutzkleidung und Equipment sowie eine klare Kommunikation. Das die Entbindung einer SARS-CoV-2 positiven Gebärenden begleitende medizinische Personal sollte auf die notwendige Anzahl an qualifizierten Beteiligten begrenzt werden, um die Anzahl der in direktem Patientenkontakt befindlichen Mitarbeiter*Innen zu reduzieren (36, 50). Das beteiligte neonatologische und anästhesiologische Team sollte frühzeitig und über den Geburtsfortschritt informiert werden, um neben der Verfügbarkeit auch die zeitliche Reserve der Ausstattung mit persönlicher Schutzausrüstung zu gewährleisten (2).
11. Eine Trennung von Mutter und gesundem Kind ist bei SARS-CoV-2 Infektion bzw. COVID-19 Erkrankung nicht zwingend erforderlich, wenn Hygieneregeln und Maßnahmen zur Vermeidung einer Virusübertragung eingehalten werden. Haut-zu-Haut Kontakt zwischen Mutter und Kind soll unter Einhaltung der Hygieneregeln und -maßnahmen (Händedesinfektion, MNS, kein Schleimhautkontakt, u.a. kein Küssen) ermöglicht werden.
Die Betreuung im Wochenbett erfolgt in Abhängigkeit von Infektionsstatus und klinischem Zustand der Mutter. Bei mildem bis moderatem Verlauf nach 10 Tagen (51, 52), bei schwereren Krankheitsverläufen nach > 14 Tagen ab Symptombeginn und negativer PCR im Naso-pharynxabstrich sind keine besonderen Maßnahmen zu treffen (2, 36, 53).
Das postpartale Vorgehen bei infektiöser Mutter (asymptomatisch oder milde COVID-19 Erkrankung) ist nach ausführlicher Aufklärung in partizipativer Entscheidungsfindung individuell und interdisziplinär festzulegen (2, 54). Inhaltlich müssen die Vorteile (Bonding, Mutter-Kind Kontakt, Stillen etc.) gegenüber dem Übertragungsrisiko, der Erkrankungswahrscheinlichkeit des Neugeborenen und nicht zuletzt der entstehenden Nachteile bei Trennung von Mutter und Kind abgewogen werden (3, 54). Das Risiko des Neugeborenen, von der Mutter mit SARS-CoV-2 infiziert zu werden, ist gering, und die Daten deuten darauf hin, dass sich das Risiko einer Infektion mit SARS-CoV-2 bei Neugeborenen nicht davon unterscheidet, ob das Neugeborene in einem separaten Raum betreut wird oder im Zimmer der Mutter bleibt (55). Bei positiv getesteten Neugeborenen ist eine Trennung von der Mutter nicht erforderlich (56).
Die WHO und die Fachgesellschaften, die diese Empfehlungen abgestimmt haben, befürworten ausdrücklich unmittelbaren Mutter-Kind-Kontakt. Die Mütter sollen zum Stillen unter adäquaten Hygienemaßnahmen, zum Haut-zu-Haut- und zum Wahrnehmen von Rooming-In-Angeboten ermutigt werden (54). Bei Rooming-In finden die konsensbasierten Empfehlungen der DGPI Berücksichtigung: Tragen eines MNS, Abstand Händehygiene, Information zu Schleim-/ Hautkontakt („Streicheln – Ja, Küssen – Nein“) (2). Neugeborene von Patientinnen mit SARS-CoV-2 Infektion sollten per Rachenabstrich (PCR) getestet und von anderen Säuglingen isoliert werden (57).
12. Stillen soll bei SARS-CoV-2 positiven Müttern ermöglicht und unterstützt werden. Bei COVID-19 Symptomatik ist die die Beratung zu spezifischen infektionsprophylaktischen Maßnahmen angezeigt.
Das Stillen wird auch bei SARS-CoV-2 Infektion der Mutter im internationalen Konsens der Fachgesellschaften befürwortet (3, 5). Das Risiko einer Übertragung von SARS-CoV-2 durch Muttermilch ist weiterhin unklar, aber unwahrscheinlich.
Seltene Einzelfallberichte über Virusnachweise (RT-PCR) in der Muttermilch lassen eine Erregerübertragung möglich erscheinen (58, 59). Ob es sich hierbei um vitale und somit infektiöse Viren handelt ist unklar (60).
Neben den bekannten Vorteilen des Stillens ist zudem ein möglicher passiver Immunschutz durch das Stillen denkbar (61). Positive Antikörpernachweise bei gleichzeitig negativer Virus- PCR aus Muttermilch von SARS-CoV-2 positiven Schwangeren (61, 62) stützen diese Hypothese.
Als Hauptübertragungsweg des Virus auf das Neugeborene während des Stillens gilt die maternale Tröpfchen- bzw. Aerosolbildung (57, 63). Eine praktische Anleitung zu den speziellen Hygieneregeln und -maßnahmen beim Stillen ist obligat (2, 3). Hierzu zählt neben Maßnahmen der Atemhygiene (MNS), die Hygiene von Händen, Brust und Milchpumpen (50). Das Abpumpen und anschließende Füttern durch eine gesunde Betreuungsperson ist z.B. bei räumlicher Trennung eine mögliche Alternative (57).
HINTERGRUNDINFORMATIONEN
zu SARS-CoV-2 und COVID-19 in der Schwangerschaft, Geburt und Wochenbett (Stand 01.10.2020)
Die Infektion mit dem erstmalig am 07.01.2020 isolierten (64, 65) Coronavirus SARS-CoV-2 ist eine hochkontagiöse Tröpfcheninfektion, die von Mensch zu Mensch (29) übertragen wird und sich binnen weniger Monate zur Pandemie ausbreitete. Zunehmende Evidenz besteht für eine mögliche systemische Inflammation mit begleitender disseminierter Gerinnungsaktivierung und Endothelbeteiligung als zentralem Pathomechanismus der COVID-19 Erkrankung (66, 67).
Prävalenz von SARS-CoV-2 Infektion/ COVID-19 Erkrankung in der Schwangerschaft
Systematische Screeninguntersuchungen weisen entsprechend der Unterschiede innerhalb der Prävalenz der Gesamtbevölkerung lokale Unterschiede auf. In den Hotspot-Regionen, wie z.B. New York City und London wiesen Untersuchungen in Entbindungskliniken 7-15 % SARS-CoV-2 positive Schwangere nach, die in bis zu 89 % asymptomatisch waren (40, 41). In Regionen mit niedrigeren COVID-19 Erkrankungsraten, wie in Connecticut (USA), fand sich im April 2020 bei Schwangeren dagegen nur eine Prävalenz von < 3 % – wiederum über 70 % davon waren asymptomatisch (68). Deutsche Daten im gleichen Zeitraum beschreiben eine vergleichbar niedrige Periodenprävalenz von 0,6 % (95 % KI 0,01 % – 3,1 %) (69).
Infektionsrisiko und Krankheitsverlauf in der Schwangerschaft
Hinweise für ein generell höheres Infektionsrisiko von SARS-CoV-2 in der Schwangerschaft existieren derzeit nicht, sodass Schwangeren die allgemeinen Maßnahmen zur Infektionsvermeidung zuzüglich der jeweils aktuell gültigen Empfehlungen des Robert Koch- Instituts für die SARS-CoV-2 Prävention empfohlen werden (8).
Das Risiko schwerer COVID-19 Ereignisse ist für Frauen allgemein weltweit geringer als bei Männern; protektiv-immunomuodulatorische und antiiflammatorische Eigenschaften werden dabei den weiblichen Steroidhormone Estradiol und Progestron zugeschrieben (70).
SARS-CoV-2 infizierte Schwangere scheinen im Vergleich zu SARS-CoV-2 infizierten Nicht-Schwangeren kein generell erhöhtes Infektionsrisiko aufzuwiesen (29, 32, 71-77).
Eine aktuelle multinationale Kohortenstudie von Schwangeren mit bestätigter SARS-CoV-2 Infektion (73 Zentren, 22 Länder) berichtet von einer Zunahme der Infektionsprävalenz mit steigendem Gestationsalter (78).
Ein erhöhtes Risiko für eine SARS-CoV-2 Infektion in der Schwangerschaft wird derzeit für bestimmte ethnische Gruppen (schwarz und hispanisch) berichtet (79-81). Im Vergleich zu nicht-hispanischen Patienten waren in einer US-amerikanischen Erhebung hispanische Patienten häufiger SARS-CoV-2 positiv (10,6 % vs. 5,5 %, aRR 1,73, 95 % KI 1,05-2,85), ebenso wie Patienten mit öffentlicher Versicherung im Vergleich zu privat Versicherten (9,5 % vs. 2,5 %, aRR 3,11; 95% KI 1,12-8,64) (82).
Das Risiko schwerer COVID-19 Verläufe von erkrankten Schwangeren liegt zwischen 5,7 und 34,8 % (83-88). Von Frauen mit COVID-19 wurde berichtet, dass etwa ein Drittel (31,5 %) der schwangeren Frauen ins Krankenhaus eingeliefert wurde, verglichen mit 5,8 % der nicht schwangeren Frauen (89). Bei SARS-CoV-2 infizierten Schwangeren, die eine COVID-19 Erkrankung entwickeln, werden zunehmend in Fallserien (75, 90-92), nationale Registerstudien (76) und Metaanalysen (30) schwere Verläufe mit relevanter mütterlicher Morbidität und Mortalität im Sinne von intensivmedizinischer Therapie- und mechanischer Beatmungsnotwendigkeit, bis hin zur Notwendigkeit einer extrakorporaler Membranoxygenierung und maternalen Todesfällen berichtet (74). Im deutschen CRONOS-Register beträgt die Anzahl wegen COVID-19 stationär aufgenommener Schwangerer unter allen mit SARS-CoV-2-Infektion registrierten Frauen 13,8%, insgesamt 5,7% erhielten eine intensivmedizinsiche Behandlung (Stand 02.10.2020).
Risikofaktoren für einen schweren Krankheitsverlauf der COVID-19 Erkrankung in der Schwangerschaft sind (77, 84, 93-95):
- maternales Alter > 35 Jahre (RR 1,78; 1.25 – 2,55; 4 Studien; n = 1058)
- hoher Body Mass Index (RR 2,38; 1,67 – 3,39; 3 Studien; n = 877)
- chronische Hypertension (RR 2,0; 1,14 – 3,48; 2 Studien; n = 858)
- vorbestehender Diabetes (RR 2,51; 1,31 – 4,80; 2 Studien; n = 858)
Für Vorerkrankungen wie Diabetes (96), Rheuma (97) und Multipler Sklerose (98) erarbeiten die jeweiligen Fachgesellschaften derzeit gesonderte Empfehlungen zur risikoadaptierten Betreuung von Schwangeren während der SARS-CoV-2 Pandemie, auch unter dem Hinblick möglicher immunsupressiver oder imunmodulatorischer Therapien.
Das Risiko intensivmedizinischer Versorgungsnotwendigkeit COVID-19 erkrankter Schwangerer wird derzeit zwischen 3 und 31,3 % berichtet (21, 30, 32, 33, 88, 94, 99-105). Dies bedeutet eine Risikoerhöhung im Vergleich zu COVID-19 erkrankten nicht-schwangeren Frauen von scheinbar kohortenunabhängig RR 1,6 95 % KI 1,3-1,9 (89) ; OR 1,62 (1,33 – 1,96) (93); OR 1,62 (95 % KI 1,33 – 1,96) (106) für die Aufnahme auf eine Intensivstation. Dieser Zusammenhang bleibt auch nach Adjustierung für Alter, zugrundeliegende Vorerkrankungen und Ethnizität erhalten (aRR 1,5, 95 % KI 1,2 – 1,8) (89).
Das Risiko einer invasiven Beatmungsnotwendigkeit COVID-19 erkrankter Schwangerer wird mit 3 – 14 % angegeben (94, 99, 104, 105). Dies bedeutet eine Risikoerhöhung im Vergleich zu COVID-19 erkrankten nicht-schwangeren Frauen von ebenfalls scheinbar kohortenunabhängig RR 1,9, 95% KI 1,4 – 2,6 (89) bzw. 1.88, 1.36 to 2.60 (93) für eine invasive Beatmungsnotwendigkeit. Dieser Zusammenhang bleibt auch nach Adjustierung für Alter, zugrundeliegenden Vorerkrankungen und Ethnizität erhalten (aRR 1.7, 95% KI 1,2 – 2,4) (89). In einer Untersuchung benötigten jedoch nur symptomatische Schwangere in 26,1 % respiratorische Unterstützung, während keine der asymptomatischen Schwangeren diese benötigte (p = 0,01) (89, 107). Als Risikofaktoren einer intensivmedizinischen Therapie-notwendigkeit (RR 4,21, 95% KI 1,06 – 16,72) und Beatmungsnotwendigkeit (RR 4,48; 95% KI 1,40 – 14,37) (93) wurden präexistente Komorbiditäten (p < 0,05) und ein mütterliches Alter > 35 Jahren (p < 0,01) (99) berichtet. Ein kausaler Zusammenhang ist jedoch nicht abschließend belegt.
Die Mortalitätsrate schwangerer Frauen mit COVID-19 im Vergleich zu nicht-schwangeren Gleichaltrigen scheint nicht generell erhöht (RR 0,8, 95% KI 0,5 – 1,3) (89) und beträgt derzeit zwischen 0,1 und 5,6 % (32, 88, 89, 93, 100, 101, 104, 108).
Maternale Todesfälle werden dabei gehäuft in Verbindung mit präexistenten Komorbiditäten, wie Adipositas, Diabetes mellitus, Asthma oder bei fortgeschrittenem maternalem Alter berichtet (88, 109). Führende maternale Todesursachen sind hierbei das akute respiratorische Distress-Sydrom (ARDS) und die schwere Pneumonie, sowie thrombembolische Ereignisse (109).
Symptomatik der SARS-CoV-2 Infektion in der Schwangerschaft
Die Symptome einer SARS-CoV-2 Infektion sind bei Schwangeren prinzipiell vergleichbar zu Nicht-Schwangeren im gebärfähigen Alter (28, 32, 110), weisen jedoch eine große klinische Variationsbreite auf (111). In Screeninguntersuchungen wurde wiederholt ein relevanter Anteil asymtpomatischer Schwangerer mit positivem SARS-CoV-2 Nachweis identifiziert (112), die Prävalenz variiert jedoch lokal in Abhängigkeit des jeweiligen Infektionsgeschehens stark (< 1 bis knapp 90 %) (113-117).
Im Erkrankungsfall werden meist (65-86 %) milde bis moderate Symptome beschrieben (32, 86, 88, 102, 108, 118). Symptomatische Infektionen waren bei Frauen im dritten Trimester der Schwangerschaft signifikant häufiger als bei Frauen im ersten Trimester der Schwangerschaft. Die Seroprävalenz war bei Frauen im ersten Trimester der Schwangerschaft und bei Frauen im dritten Trimester ähnlich, was auf ein ähnliches Infektionsrisiko schließen lässt, aber der Anteil der Frauen mit Symptomen und der Anteil der Frauen, die einen Krankenhausaufenthalt benötigten, waren in der Gruppe des dritten Trimesters höher als in der Gruppe des ersten Trimesters (119).
Die häufigsten Symptome bei SARS-CoV-2 infizierten Schwangeren sind Husten und Fieber (120) (siehe Tabelle 1), wobei diese jedoch im Vergleich zu Nicht-Schwangeren seltener auftreten (87).
Im deutschen CRONOS-Register finden sich 37% asymptomatische Frauen. Husten wurde bei 38% als Symptom angegeben, gefolgt von allgemeinem Krankheitsgefühl (34%), Müdigkeit (28%), Geruchs- und Geschmacksveränderungen (27%) sowie Fieber (25%), Halsschmerzen (24%) und Schnupfen/Nasale Obstruktion (22%) (Stand 02.10.2020).
Tabelle 1: Symptome der COVID-19 Erkrankung nach (28) und (93)

Komplikationen in der Schwangerschaft
Fehlgeburten traten während der SARS-CoV-2 Pandemie bisher nicht häufiger auf, die Datenlage ist aber für eine abschließende Beurteilung weiterhin unzureichend (28, 123-125). Jedoch kann auch bei Fehlgeburten an eine Erstmanifestation einer SARS-CoV-2 Infektion gedacht werden (126). In zwei aktuellen multinationale Kohortenstudien von Schwangeren mit bestätigter SARS-CoV-2 Infektion liegt die Fehlgeburtenrate bei 2,3 % (78) bzw. 2,2 % (105).
Plazentainsuffizienz und Fetale Wachstumsrestriktion
Es gibt bisher nur begrenzte Daten, ob eine fetale Wachstumsrestritktion (FGR) eine unmittelbare Folge einer Infektion mit SARS-CoV-2 sein kann. Bisherige Empfehlungen stützen sich auf Beobachtungen vormaliger MERS-Infektionen, in deren Rahmen zwei Drittel der Schwangerschaften von FGR betroffen waren. In einigen COVID-19 Fallserien werden fetale Wachstumsrestriktionen berichtet (127).
In histologischen Untersuchungen (12) COVID-19 erkrankter Schwangerer wurden postpartal Hinweise uteroplazentarer vaskulärer Malperfusion, einschließlich akuter und chronischer intervillöser Inflammation, fokaler avaskulärer Villiitis sowie Thromben in größeren fetalen Gefäßen der Chorionplatte und von Stammvilli gefunden (117, 128-130). Ein aktuelles Review berichtet sowohl fetale (35,3 %; 95 % KI 27,7 – 43,0 %) als auch maternale (46 %; 95 % KI 38,0 – 54,0 %) vaskuläre Malperfusionszeichen mit Hinweisen für intraplazentare Inflammation (Villiitis 8,7 %, Intervillosiitis 5,3 %, Chorioamnionitis 6 %), bei jedoch nur 21 % SARS-CoV-2 Positivität der Plazenten (131). Auch wenn solche histomorphologischen Veränderungen nicht universell nachweisbar sind (130, 132), und nicht klar ist, ob die beschriebenen plazentaren Läsionen durch COVID-19 bedingte Koagulopathie, Endotheliitis, Hypoxie im Rahmen exazerbierter maternaler Erkankung, direkter viraler plazentarer Infektion oder einer Kombination dieser Möglichkeiten verursacht wird, ist eine plazentare Unterversorgung mit resultierender FGR im Rahmen einer maternalen COVID-19 Infektion derzeit nicht auszuschließen.
SARS-CoV-2 in der Schwangerschaft ist mit einer erhöhten Präeklampsie-Prävalenz (ca. 5,9 % bis 10,5 %) assoziiert (88, 101, 133). Im Vergleich zu gematchten nicht-schwangeren SARS-CoV-2 positiven Frauen berichtet eine aktuelle schwedische Arbeit ein erhöhtes Präeklampsierisiko von RR 1,84 (95 % KI 1,004 – 3,36) für Schwangere mit SARS-CoV-2. Die berichteten kardiovaskulärer Komplikationen einer SARS-CoV-2 Infektion lassen dabei eine signifikante Wirkung des Virus auf das mütterliche Gefäßsystem vermuten (134). Ebenso können inflammatorische Veränderungen bei COVID-19 Erkankung mit hypoxischen Veränderungen in der Plazenta und einem sich entwickelnden präeklamptischen Zustand assoziiert sein (135).
Die Frühgeburtenraten bei COVID-19 erkrankten Schwangeren variieren je nach Studie zwischen 6 % und 39 % (87, 93, 100, 103, 104, 108, 136, 137). Damit ist die im Vergleich zu nicht-infizierten Schwangeren erhöht OR 3,01, 95 % KI 1,16 – 7,85 (106). Die Raten von Frühgeburten waren in den US-Studien (12 %) im Vergleich zu chinesischen (17 %) und europäischen Studien (19 %) am niedrigsten. Das deutsche CRONOS Register berichtet zum 02.10.2020 auf der Basis von 185 entbundenden Patientinnen eine Rate von 14,0 % Frühgeburten, wovon ca. Dreiviertel nach der 34. SSW geboren haben (34).
In einer retrospektiven Querschnittsstudie (New York) zeigte sich die Frühgeburtenrate während eines Krankenhausaufenthaltes aufgrund einer SARS-CoV-2 Infektion bei Frauen, die in der frühen Frühgeburtsperiode (23+0 bis 33+6 SSW) diagnostiziert wurden, signifikant niedriger als bei Frauen, die in der späten Frühgeburtsperiode (34+0 bis 36+6 SSW) diagnostiziert wurden (7/36 [19,4 %] vs. 18/29 [62 %], p = 0,001) (132).
Ob die berichteten Frühgeburtsraten iatrogen durch kritischen maternalen Zustand bedingt sind oder aber spontane Frühgeburten darstellen, ist in den frühen Fallserien nicht ausreichend differenziert worden (138). Regional wird von einem iatrogenen Anteil von bis zu 94 % der Frühgeburten (bei einer beobachteten Frühgeburtenrate von 17 %) berichtet (93). Gemäß aktueller systematischen Reviews (93, 99) wird bei an COVID-19 erkrankten Schwangeren keine erhöhte Rate an spontanen Frühgeburten beobachtet, der Anteil anderweitiger Frühgeburten ist jedoch größer.
Die aktuelle Auswertung der britischen UKOSS-Registerdaten (32) zeigt eine Frühgeburtsrate von 27 % (47 % iatrogen aufgrund mütterlicher Beeinträchtigung, 15 % iatrogen aufgrund fetaler Beeinträchtigung).
In den bisherigen COVID-19 Fallserien werden vereinzelt vermehrte Intrauterine Fruchttode berichtet (127). Aktuelle britische Veröffentlichungen verzeichnen ansteigende Raten an Totgeburten (11, 5 vs. 4,1 per 1000 Geburten) im Vergleich zu präpandemischen Zeiträumen (139). In Detuschland wurden bisher nur 2 Totgeburten und 4 Aborte, davon ein Spätabort in CRONOS registriert (34)
Psychosoziale Belastungen durch die Pandemie und Containmentmaßnahmen
Zunehmende Ängstlichkeit und Depressivität von Schwangeren während der SARS-CoV-2 Pandemie mit teils höheren Raten der psychologischen Folgen im Vergleich der Zahl klinisch vom Virus betroffenen Patientinnen sind vielfältig berichtet worden (140-143). Eine Sensibilisierung für psychische Pathologien in Schwangerschaft und Wochenbett im Rahmen der Pandemie sowie mögliche Screeningmaßnahmen werden diskutiert.
Seit Beginn der SARS-CoV-2 Pandemie und den begleitenden Containment- und Lockdown-Maßnahmen ist auch eine Abnahme der schwangerschaftsspezifischen Notfallkonsultationen (z.T. bis zu 28,5 % (95 % KI 27,2 – 29,9) berichtet worden (144, 145). Unter dem Aspekt zunehmender Ängstlichkeit und vereinzelter, wenn auch nicht beweisbar im Zusammenhang hiermit stehenden, erhöhten Raten intrauteriner Fruchttode (139, 144) sollten Schwangere anhaltend ermutigt werden, sowohl Angebote im Rahmen der Mutterschaftsvorsorge als auch entsprechende Notfallhilfe wahrzunehmen. Dies gilt uneingeschränkt auch für die Empfehlungen der STIKO zur Impfung in der Schwangerschaft, mit besonderer Berücksichtigung von Influenza und Pertussis.
Thombembolierisiko
COVID-19 kann als eine prothrombotische Erkrankung angesehen werden, eine hohe Anzahl thrombotischer Episoden ist bislang im Zusammenhang mit COVID-19 Erkrankungen sowie ein Überlebensvorteil einer Heparintherapie berichtet worden. Unter Anwendung der Virchow-Trias sind Anomalien im vaskulären Endothel, ein veränderter Blutfluss und Anomalien der Thrombozytenfunktion, die zu venösen und arteriellen Thrombosen führen im Rahmen der COVID-19 Erkrankung diskutiert worden (146). Die Risikostratifizierung von COVID-19 assoziierten Thrombosen sollte daher individuell erfolgen und neben dem Alter, das Vorhandensein von Vorerkrankungen und die klinische Erkrankungsschwere einer SARS-CoV-2 Infektion berücksichtigen. Eine Verringerung der körperlichen Aktivität infolge von Containment- oder Isolationsmaßnahmen (147) sollte als möglicher additiver Risikofaktor Berücksichtigung finden. Bei Hospitalisierung oder schwerer COVID-19 Ekrankung besteht ein Risiko für pulmonale thromboembolische Komplikationen durch mindestens zwei verschiedene Mechanismen – immunmodulierte und krankenhausassoziierte venöse Thromboembolien (19, 148).
Wiederholt wurden thrombembolische Komplikationen einer COVID-19 Erkrankung in der Schwangerschaft berichtet (21). Ein thrombembolisches Ereignis kann auch die Erstmanifestation einer COVID-19 Erkrankung in der Schwangerschaft darstellen (149-151). Im Vergleich zu nicht-schwangeren Frauen mit COVID-19 zeigt sich kein erhöhtes Risiko für eine krankenhausbedingte Thrombose (19).
Vertikale Transmission
In der Diskussion des Begriffes „vertikale“ Übertragung ist ein Unterscheidung zwischen intrauteriner und intrapartaler/postnataler Übertragung von SARS-CoV-2, wenn dies möglich ist, empfohlen (152). Bis zum jetzigen Zeitpunkt sind keine allgemeingültigen Aussagen zur vertikalen Transmission des Virus von Mutter zum Ungeborenen zu treffen (153). Erste Untersuchungen sahen keinen schlüssigen Beweis für die relevante vertikale Mutter-Kind-Übertragung (154, 155). In neueren Übersichtsarbeiten werden sowohl die prinzipielle Möglichkeit einer vertikalen Transmission als auch mögliche pathophysiologische Mechanismen diskutiert. Es existieren vereinzelte gut dokumentiert Fallberichte möglicher vertikaler Transmissionen (128, 156, 157), deren klinische Signifikanz jedoch weiterhin unklar bleibt. Über eine mögliche vertikale Übertragung wurde in mehreren Fällen einer peripartalen mütterlichen Infektion berichtet (85, 158-160), was darauf hindeutet, dass eine kongenitale Infektion möglich, aber selten ist (< 3 % der mütterlichen Infektionen) (161). Man geht davon aus, dass die meisten Infektionen bei Neugeborenen aerosolbedingt sind.
Zunächst sprachen ein fehlender Virusnachweis in Fruchtwasser, Vaginalsekret oder Nabelschnurblut SARS-CoV-2 (136) eher gegen eine mögliche Transmission. Einzelnachweise (162) von SARS-CoV-2 im Nabelschnublut (161), Vaginalsekret (124, 163) und Fruchtwasser (128) liegen nun vor. Auch wurden Antikörper gegen SARS-CoV-2 im Nabelschnurblut nachgewiesen, die transplazentar übergetreten sein könnten (164, 165).
Die Häufigkeit einer SARS-CoV-2 Virämie ist als äußerst niedrig (1 Studie, < 1 %) und transient beschrieben worden (166), was eine Transmission auf hämatogenem Wege unwahrscheinlich macht. Eine hohe SARS-CoV-2 Viruslast in der Plazenta wurde in Verbindung mit einer mütterlichen Virämie und gefolgt von einer neonatalen Infektion als wahrscheinliche vertikale Transmission beschrieben (156). Plazentar wurden neben Virus-RNA (167, 168) auch elektronenmikrsokopisch Viren in den Syncytiotrophoblastzotten nachgewiesen (156, 169). Als möglicher Pathomechanismus transplazentarer viraler Transmission wird der Expressionsnachweis (169-175) von ACE2R und TMPRSS2 im Syncytiotrophoblasten als Eintrittsmechanismus für das SARS-CoV-2 Virus angesehen. Eine möglich protektive physiologische Barrierefunktion mit immunomodulatorischen Eigenschaften der Plazenta gegen den Virusübertritt wird diskutiert (176, 177). Es besteht keine klare Evidenz für den transplazentaren Virusübertritt ins Fruchtwasser (178).
Das theoretische Risiko einer intrauterinen Infektion oder einer peripartalen Infektion während der Geburt bei Neugeborenen ist biologisch plausibel. Das Ausmaß dieses mutmaßlichen Risikos kann jedoch in den verschiedenen Stadien der Schwangerschaft aufgrund mehrerer Variablen (physiologische Veränderungen der Plazenta, Expression der Virusrezeptoren oder Entbindungsweg) variieren (179). Eine vertikale Übertragung im Rahmen der schweren COVID-19 Erkrankung ist möglich und scheint in einer Minderheit der Fälle im dritten Trimester aufzutreten. Angesichts des Mangels an Daten aus den frühen Trimestern kann jedoch keine Bewertung der vertikalen Übertragungsraten in der Frühschwangerschaft und des potenziellen Risikos für die daraus resultierende fetale Morbidität und Mortalität vorgenommen werden (161).
Zusammenfassend wurde eine mögliche vertikale Übertragung von SARS CoV-2 derzeit in einigen Fallberichten (180, 181) beobachtet und in Übersichtsarbeiten (182) diskutiert. Neonatale SARS-CoV-2 Infektionen sind selten, selten symptomatisch, und die Infektionsrate ist nicht höher, wenn das Kind vaginal geboren wird, gestillt wird oder bei der Mutter verbleibt (183).
SARS-CoV-2 und COVID-19 Diagnostik in der Schwangerschaft
Die Diagnose einer Infektion mit SARS-CoV-2 bzw. der Erkrankung COVID-19 erfolgt bei Schwangeren in Analogie zur Allgemeinbevölkerung. Die derzeit etablierten Diagnosemethoden umfassen den Nachweis viraler RNA oder viraler Antigene in geeigneten respiratorischen Proben, spezifischer Antikörper im Blut sowie typischer CT-morphologischer Befunde der Lunge (184). Ein Screening asymptomatischer Schwangerer wird je nach Prävalenz aufgrund der relevanten Anteile asymptomatisch infizierter Schwangerer bei z.B. Hospitalisierung oder Entbindung diskutiert.
Die CT-Untersuchung ist der Goldstandard in der Bildgebung (Sensitivität 97 %) und wird bei schwangeren Frauen mit Verdacht auf COVID-19 vereinzelt als primärer Nachweis von COVID-19 in epidemischen Gebieten angesehen (185, 186). In Regionen niedrigerer Inzidenz sollte diese, aufgrund der Reststrahlenbelastung, symptomatischen Schwangeren, zur Differentialdiagnostik oder zum Ausschluss von Komplikationen, vorbehalten bleiben und nicht als allgemeines Screeningsinstrument dienen (187). Bilaterale pneumonische Veränderungen (57,9 %) und Milchglastrübungen (65,8 %) werden typischerweise berichtet (101). Eine Metaanalyse zeigte CT-Veränderungen bei 71 % der COVID-19 erkrankten Schwangeren (87).
Die Verwendung von Lungenultraschall wurde als prädiktiver für eine SARS-CoV-2 Infektion erachtet als die ausschließliche Verwendung der Symptomatik (188). Derzeit fehlt eine abschließende Validierung, wohingegen die Untersuchung zusätzliche personelle Ressourcen bindet und Personal zusätzlich einer möglichen Transmission exponiert (189). Die Sonographie der Lunge sollte daher derzeit nicht als Alternative zur CT zur Beurteilung einer COVID-19 Pneumonie bei schwangeren Frauen betrachtet werden (190).
Die Labordiagnostik im Rahmen einer COVID-19 Erkrankung in der Schwangerschaft ist wenig diagnosebildend. Die häufigsten Laborveränderungen sind neben einer Lymphozytopenie und CRP-Erhöhung, eine Erhöhung von Procalcitonin und Transaminasen (93, 99, 101) (s. Tabelle 2). Die diagnostische Wertigkeit der Lymphozytopenie in der Schwangerschaft wird im Zusammenhang mit SARS-CoV-2 kritisch diskutiert (191).
Tabelle 2: Labordiagnostische Veränderungen nach (93, 99, 101)
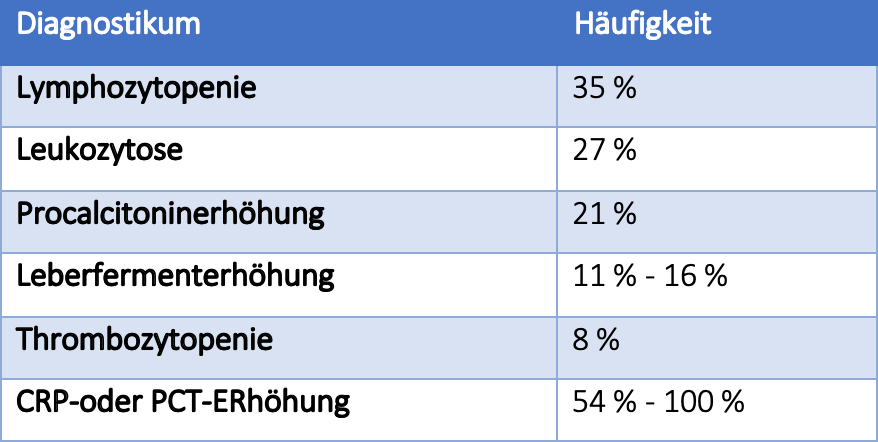
Die laborchemischen Merkmale schwangerer Frauen mit COVID-19 Erkrankung zeigen sich vielfältig und atypisch (192). Die Laboruntersuchung von SARS-CoV-2 positiven schwangeren Frauen zum Zeitpunkt der Diagnose kann Patientinnen mit einem Risiko für einen Aufenthalt auf der Intensivstation identifizieren (niedrigere Lymphozytenzahl) (193).
Hinsichtlich des thrombembolischen Komplikationsrisikos sollte neben der Bestimmung von D-Dimeren, Prothrombinzeit und Thrombozytenzahl bei allen Patientinnen, die mit COVID-19 behandelt werden, in der Schwangerschaft zusätzlich die Überwachung der aktivierten partiellen Thromboplastinzeit (aPTT) und der Fibrinogenspiegel in Betracht gezogen werden (194).
Differentialdiagnostisch ist bei Schwangeren mit COVID-19 Erkrankung eine Überschneidung zu typischen Symptomen von Schwangerschaftskomplikationen zu berücksichtigen. Klinische und laborchemische Manifestationen können ein HELLP-Syndrom imitieren (195-197). Komplexe Interaktionen in Symptomatik und Prävalenz müssen auch zwischen SARS-CoV-2 Infektion und hypertensiven Schwangerschaftserkrankungen berücksichtigt werden (198). Herzerkrankungen und COVID-19 haben ebenfalls gemeinsame Symptome, die in der Schwangerschaft zu einer Fehldiagnose führen können (199). Geburtshilfliche Differentialdiagnosen sollten in jeder Abklärung einer vermuteten COVID-19 Erkrankung berücksichtigt werden (200).
COVID-19 Therapie in der Schwangerschaft
Eine spezifische antivirale Therapie ist derzeit nicht generell empfohlen (26). Die Erwägung und Prüfung des Einsatzes antiviraler Medikation sollte jedoch auch bei schwangeren COVID-19 Patientinnen in Abhängigkeit der Schwere des Krankheitsbildes individuell erfolgen (201).
In Fallberichten (202) wurden und werden schwangere COVID-19 Patientinnen mit Remdesivir , einem Nukleotidanalogon mit in-vitro Aktivität gegen SARS-CoV-2 (153), oder anderen Wirkstoffen (Oseltamivir, Lopinavir-Ritonavir, Hydroxychloroquin, Chloroquin) unter Studienbedingungen oder im Rahmen von Einzelfallentscheidungen behandelt (32). Jedoch schließen nur wenige Studien schwangere Frauen ein, wie z.B. die SOLIDARITY-Studie und die RECOVERY-Studie (108).
Remdesivir wurde bereits bei schwangeren Frauen mit Ebola- und Marburg-Virus-Infektion angewendet, zeigte hierbei keine fetale Toxizität (203). Es ist nachweislich mit einer Verkürzung der Zeit bis zur klinischen Besserung bei Personen mit schwerer COVID-19 Erkrankung assoziiert (204). Remdesivir kann daher zur Behandlung von schwangeren Patientinnen mit schwerer COVID-19 Erkrankung auf der Basis einer Einzelfallentsscheidung eingesetzt werden.
Frühe Daten randomisierter Studien zeigen keinen Nutzen von Hydroxychloroquin oder Chloroquin. Unerwünschte mütterlichen Wirkungen beinhalten Herzrhythmusstörungen (QT-Intervallverlängerung und ventrikuläre Tachykardie) (205). Für Hydroxychloroquin wurde eine leichte Erhöhung des fetalen Malformationsrisikos bei Applikation im ersten Trimenon berichtet (aRR 1,26; 95 % KI 1,04 – 1,54). Eine Erhöhungen des Risikos für orale Spaltbildungen, respiratorische und urogenitale Anomalien wurde hierbei beobachtet (206).
Andere derzeit im experimentellen Einsatz bei SARS-CoV-2 Infektionen befindliche Wirkstoffe kommen aufgrund ihrer Teratogenität nicht für den Einsatz an Schwangeren in Betracht (Ribavirin, Baricitinib) (17).
Eine antibiotische Therapie soll früh bei vermuteter oder bestätigter bakterieller Superinfektion möglichst erreger- und resistenzgerecht erfolgen (26).
Die Applikation von Steroiden aus maternaler Indikation sollte auch bei schwangeren COVID-19 Patientinnen mit Sauerstoffbedarf in erwogen werden, da erste Zwischenergebnisse der RECOVERY-Studie eine signifikante Verringerung der Mortalität zeigen konnte (207). Diese Empfehlung fand bereits Einzug in die britischen Richtlinien (208). Das RECOVERY-Studienprotokoll für Schwangere empfiehlt Prednisolon 40 mg oral einmal täglich bzw. Hydrocortison 80 mg intravenös zweimal täglich (209).
Die Pausierung einer bestenden Einnahme von ASS aus schwangerschaftsspezifischen Gründen wird diskutiert (210). Bei relevanter Thrombozytopenie (< 50 Gpt/l) ist die Pausierung aufgrund steigender Blutungsrisiken, auch hinsichtlich geburtshilflicher und anästhesiologischer Aspekte, angeraten (45).
Redaktionsgruppe (Reihenfolge alphabetisch)
Dr. Carsten Hagenbeck, Prof. Dr. Kurt Hecher, PD Dr. Ulrich Pecks, PD Dr. Dietmar Schlembach, Prof. Dr. Ekkehard Schleußner*, Prof. Dr. Rolf Schlösser, Dr. Janine Zöllkau
*Korrespondierender Autor
Verantwortlich von Seiten der DGPI: Prof. Dr. Arne Simon, Prof. Dr. Johannes Hübner, Prof. Dr. Reinhard Berner, Prof. Dr. Markus Knuf, Prof. Dr. Markus Hufnagel
Verantwortlich von Seiten der NKS: Prof. Dr. Michael Abou-Dakn
Mit ganz herzlichem Dank an alle, die sich an der Erstellung aktiv beteiligt haben.
Literatur
- DGGG. Empfohlene Präventionsmaßnahmen für die geburtshilfliche Versorgung in deutschen Krankenhäusern und Kliniken im Zusammenhang mit dem Coronavirus 16.03.2020. 2020 [updated 03/16/2020. Available from: https://www.dggg.de/fileadmin/documents/Weitere_Nachrichten/2020/COVID-19_DGGG-Empfehlungen_fuer_Kreissaele_20200319_f.pdf.
- DGPI. Umgang mit Neugeborenen SARS-CoV-2 positiver Mütter mit oder ohne klinische Erkrankung (COVID-19) 2020 [updated 03/31/2020. Available from: https://dgpi.de/stellungnahme-dgpi-dggg-dgpm-umgang-mit-neugeborenen-sars-cov-2-positiver-muetter/.
- Stillkommission N. Stillen und COVID-19 – Stellungnahme der Nationalen Stillkommission vom 11. März 2020 2020 [updated 03/11/2020. Available from: https://www.mri.bund.de/de/themen/nationale-stillkommission/stellungnahmen/stillen-covid-19/.
- Zollkau J, Hagenbeck C, Hecher K, Pecks U, Schlembach D, Simon A, et al. [Update on Recommendations for SARS-CoV-2/COVID-19 During Pregnancy, Birth and Childbed]. Z Geburtshilfe Neonatol. 2020;224(4):217-22.
- Cochrane. COVID-19 review of national clinical practice guidelines for key questions relating to the care of pregnant women and their babies: Cochrane; 2020 [International Consensus]. Available from: https://pregnancy.cochrane.org/news/covid-19-review-national-clinical-practice-guidelines-key-questions-relating-care-pregnant.
- RKI. Erweiterte Hygienemaßnahmen im Gesundheitswesen im Rahmen der COVID-19 Pandemie 2020 [updated 05/13/2020. Available from: https://www.rki.de/DE/Content/InfAZ/N/Neuartiges_Coronavirus/erweiterte_Hygiene.html.
- Boelig RC, Saccone G, Bellussi F, Berghella V. MFM guidance for COVID-19. Am J Obstet Gynecol MFM. 2020:100106.
- RKI. COVID-19 (Coronavirus SARS-CoV-2) 2020 [updated 06222020. Available from: https://www.rki.de/DE/Content/InfAZ/N/Neuartiges_Coronavirus/nCoV.html.
- Jamieson DJ, Steinberg JP, Martinello RA, Perl TM, Rasmussen SA. Obstetricians on the Coronavirus Disease 2019 (COVID-19) Front Lines and the Confusing World of Personal Protective Equipment. Obstet Gynecol. 2020;135(6):1257-63.
- Kagan KO, Chaoui R. Ultraschall in der Schwangerschaft wahrend der Corona-Virus Pandemie: Ein praktisches Vorgehen. Ultraschall Med. 2020.
- Bourne T, Leonardi M, Kyriacou C, Al-Memar M, Landolfo C, Cibula D, et al. ISUOG Consensus Statement on rationalization of gynecological ultrasound services in context of SARS-CoV-2. Ultrasound Obstet Gynecol. 2020;55(6):879-85.
- Shanes ED, Mithal LB, Otero S, Azad HA, Miller ES, Goldstein JA. Placental Pathology in COVID-19. Am J Clin Pathol. 2020.
- CDC. Interim Considerations for Infection Prevention and Control of Coronavirus Disease 2019 (COVID-19) in Inpatient Obstetric Healthcare Settings 2020.
- McIntosh JJ. Corticosteroid Guidance for Pregnancy during COVID-19 Pandemic. Am J Perinatol. 2020;37(8):809-12.
- D’Souza R, Ashraf R, Rowe H, Zipursky J, Clarfield L, Maxwell C, et al. Pregnancy and COVID-19: Pharmacologic Considerations. Ultrasound Obstet Gynecol. 2020.
- Schleussner E. The prevention, diagnosis and treatment of premature labor. Dtsch Arztebl Int. 2013;110(13):227-35; quiz 36.
- Berghella V. Coronavirus disease 2019 (COVID-19): Pregnancy issues UpToDate®: UpToDate, Inc. ; 2020 [updated May 27, 2020. Literature review current through: Apr 2020:[Available from: https://www.uptodate.com/contents/coronavirus-disease-2019-covid-19-pregnancy-issues?search=covid%2019%20pregnancy&source=search_result&selectedTitle=1~150&usage_type=default&display_rank=1.
- Bikdeli B, Madhavan MV, Jimenez D, Chuich T, Dreyfus I, Driggin E, et al. COVID-19 and Thrombotic or Thromboembolic Disease: Implications for Prevention, Antithrombotic Therapy, and Follow-Up: JACC State-of-the-Art Review. J Am Coll Cardiol. 2020;75(23):2950-73.
- D’Souza R, Malhame I, Teshler L, Acharya G, Hunt BJ, McLintock C. A critical review of the pathophysiology of thrombotic complications and clinical practice recommendations for thromboprophylaxis in pregnant patients with COVID-19. Acta Obstet Gynecol Scand. 2020.
- RCOG. Coronavirus (COVID-19) Infection in Pregnancy 2020 [updated 06/04/2020. Version 10:[Available from: https://www.rcog.org.uk/globalassets/documents/guidelines/2020-06-04-coronavirus-covid-19-infection-in-pregnancy.pdf.
- Kadir RA, Kobayashi T, Iba T, Erez O, Thachil J, Kazi S, et al. COVID-19 Coagulopathy in Pregnancy: Critical Review, Preliminary Recommendations and ISTH Registry – Communication from the ISTH SSC for Women’s Health. J Thromb Haemost. 2020.
- Thachil J, Tang N, Gando S, Falanga A, Cattaneo M, Levi M, et al. ISTH interim guidance on recognition and management of coagulopathy in COVID-19. J Thromb Haemost. 2020;18(5):1023-6.
- Iba T, Levy JH, Levi M, Connors JM, Thachil J. Coagulopathy of Coronavirus Disease 2019. Crit Care Med. 2020;48(9):1358-64.
- Donders F, Lonnee-Hoffmann R, Tsiakalos A, Mendling W, Martinez de Oliveira J, Judlin P, et al. ISIDOG Recommendations Concerning COVID-19 and Pregnancy. Diagnostics (Basel). 2020;10(4).
- Stephens AJ, Barton JR, Bentum NA, Blackwell SC, Sibai BM. General Guidelines in the Management of an Obstetrical Patient on the Labor and Delivery Unit during the COVID-19 Pandemic. Am J Perinatol. 2020.
- RCOG TRCoOaG. Coronavirus (COVID-19) Infection in Pregnancy
Information for healthcare professionals 2020 [Available from: https://www.rcog.org.uk/globalassets/documents/guidelines/2020-07-24-coronavirus-covid-19-infection-in-pregnancy.pdf.
- Oxford-Horrey C, Savage M, Prabhu M, Abramovitz S, Griffin K, LaFond E, et al. Putting It All Together: Clinical Considerations in the Care of Critically Ill Obstetric Patients with COVID-19. Am J Perinatol. 2020;37(10):1044-51.
- Elshafeey F, Magdi R, Hindi N, Elshebiny M, Farrag N, Mahdy S, et al. A systematic scoping review of COVID-19 during pregnancy and childbirth. Int J Gynaecol Obstet. 2020.
- Wu Z, McGoogan JM. Characteristics of and Important Lessons From the Coronavirus Disease 2019 (COVID-19) Outbreak in China: Summary of a Report of 72314 Cases From the Chinese Center for Disease Control and Prevention. JAMA. 2020.
- Capobianco G, Saderi L, Aliberti S, Mondoni M, Piana A, Dessole F, et al. COVID-19 in pregnant women: A systematic review and meta-analysis. Eur J Obstet Gynecol Reprod Biol. 2020;252:543-58.
- Dubey P, Reddy SY, Manuel S, Dwivedi AK. Maternal and neonatal characteristics and outcomes among COVID-19 infected women: An updated systematic review and meta-analysis. Eur J Obstet Gynecol Reprod Biol. 2020;252:490-501.
- Knight M, Bunch K, Vousden N, Morris E, Simpson N, Gale C, et al. Characteristics and outcomes of pregnant women admitted to hospital with confirmed SARS-CoV-2 infection in UK: national population based cohort study. BMJ. 2020;369:m2107.
- Remaeus K, Savchenko J, Brismar Wendel S, Gidlof SB, Graner S, Jones E, et al. Characteristics and short-term obstetric outcomes in a case series of 67 women tested positive for SARS-CoV-2 in Stockholm, Sweden. Acta Obstet Gynecol Scand. 2020.
- Mario Rüdiger UP. CRONOS Newsletter 08. 2020.
- Ferrazzi E, Frigerio L, Savasi V, Vergani P, Prefumo F, Barresi S, et al. Vaginal delivery in SARS-CoV-2 infected pregnant women in Northern Italy: a retrospective analysis. BJOG. 2020.
- Edward Morris POB, Gemma Goodyear, Sophie Relph, Jennifer Jardine, Anita Powell, Emma Gilgunn-Jones, Ed Mullins, Russell Viner, David Evans, Mary Ross-Davie. Coronavirus (COVID-19) Infection in Pregnancy – Information for healthcare professionals 2020 [updated 05/13/2020. Available from: https://www.rcog.org.uk/globalassets/documents/guidelines/2020-05-13-coronavirus-covid-19-infection-in-pregnancy.pdf.
- Gracia-Perez-Bonfils A, Martinez-Perez O, Llurba E, Chandraharan E. Fetal heart rate changes on the cardiotocograph trace secondary to maternal COVID-19 infection. Eur J Obstet Gynecol Reprod Biol. 2020;252:286-93.
- Barth RE, De Regt MJA. Persistence of viral RNA in stool samples from patients recovering from covid-19. BMJ. 2020;369:m1724.
- Amirian ES. Potential fecal transmission of SARS-CoV-2: Current evidence and implications for public health. Int J Infect Dis. 2020;95:363-70.
- Sutton D, Fuchs K, D’Alton M, Goffman D. Universal Screening for SARS-CoV-2 in Women Admitted for Delivery. N Engl J Med. 2020.
- Khalil A, Hill R, Ladhani S, Pattisson K, O’Brien P. SARS-CoV-2 in pregnancy: symptomatic pregnant women are only the tip of the iceberg. Am J Obstet Gynecol. 2020.
- e.V. DGfA-uV. COVID-19 Empfehlung der DGAV e.V. 2020 [updated 04/24/2020. Available from: https://www.awmf.org/regelwerk/.
- e.V. PDGfGuG. DGGG EMPFIEHLT: VÄTER BEI DER GEBURT ZULASSEN – AUCH IN ZEITEN DER CORONA-PANDEMIE 2020 [Pressemitteilung der DGGG]. Available from: https://www.dggg.de/presse/pressemitteilungen-und-nachrichten/dggg-empfiehlt-vaeter-bei-der-geburt-zulassen-auch-in-zeiten-der-corona-pandemie.
- Peter Kranke SW, Magdalena Sitter, Patrick Meybohm, Thierry Girard. Obstetric Anesthesia During the SARS-CoV-2 Pandemic – a Brief Overview of Published Recommendations for Action by National and International Specialist Societies and Committees. Anästhesiol Intensivmed Notfallmed Schmerzther. 2020;55(04):266-74.
- Morau E, Bouvet L, Keita H, Vial F, Bonnet MP, Bonnin M, et al. Anaesthesia and intensive care in obstetrics during the COVID-19 pandemic. Anaesth Crit Care Pain Med. 2020;39(3):345-9.
- Landau R. COVID-19 Pandemic and Obstetric Anaesthesia. Anaesth Crit Care Pain Med. 2020;39(3):327-8.
- Bauer ME, Bernstein K, Dinges E, Delgado C, El-Sharawi N, Sultan P, et al. Obstetric Anesthesia During the COVID-19 Pandemic. Anesth Analg. 2020;131(1):7-15.
- Mihaela Podovei KB, Ronald George, Ashraf Habib, Rachel Kacmar, Brian Bateman and Ruth Landau. Interim Considerations for Obstetric Anesthesia Care related to COVID19 [PDF]. 2020 [updated 05/22/2020. Available from: soap.org.
- WHO. Q&A: Pregnancy, childbirth and COVID-19 2020 [updated 18 March 2020 Available from: https://www.who.int/emergencies/diseases/novel-coronavirus-2019/question-and-answers-hub/q-a-detail/q-a-on-covid-19-pregnancy-and-childbirth.
- ACOG. Novel Coronavirus 2019 (COVID-19) 2020 [updated 05/19/2020. Available from: https://www.acog.org/clinical/clinical-guidance/practice-advisory/articles/2020/03/novel-coronavirus-2019.
- Wolfel R, Corman VM, Guggemos W, Seilmaier M, Zange S, Muller MA, et al. Virological assessment of hospitalized patients with COVID-2019. Nature. 2020;581(7809):465-9.
- Arons MM, Hatfield KM, Reddy SC, Kimball A, James A, Jacobs JR, et al. Presymptomatic SARS-CoV-2 Infections and Transmission in a Skilled Nursing Facility. N Engl J Med. 2020;382(22):2081-90.
- RKI. SARS-CoV-2 Steckbrief zur Coronavirus-Krankheit-2019 (COVID-19). 2020.
- (WHO) WHO. Clinical management of severe acute respiratory infection (SARI) when COVID-19 disease is suspected, interim guidance 27 May 2020 2020 [Available from: https://www.who.int/health-topics/coronavirus#tab=tab_1.
- CDC. Care for newborns. 2020 [Available from: https://www.cdc.gov/coronavirus/2019-ncov/hcp/caring-for-newborns.html
- ACOG. Summary of Key Updates (September 25,2020). 2020.
- CDC. Coronavirus Disease 2019 (COVID-19) Evaluation and Management Considerations for Neonates At Risk for COVID-19. 2020 [Available from: https://www.cdc.gov/coronavirus/2019-ncov/hcp/caring-for-newborns.html.
- Cui Y, Tian M, Huang D, Wang X, Huang Y, Fan L, et al. Corrigendum to: A 55-Day-Old Female Infant Infected With 2019 Novel Coronavirus Disease: Presenting With Pneumonia, Liver Injury, and Heart Damage. J Infect Dis. 2020.
- Gross R, Conzelmann C, Muller JA, Stenger S, Steinhart K, Kirchhoff F, et al. Detection of SARS-CoV-2 in human breastmilk. Lancet. 2020.
- Chambers C, Krogstad P, Bertrand K, Contreras D, Tobin NH, Bode L, et al. Evaluation for SARS-CoV-2 in Breast Milk From 18 Infected Women. JAMA. 2020.
- Dong Y, Chi X, Hai H, Sun L, Zhang M, Xie WF, et al. Antibodies in the breast milk of a maternal woman with COVID-19. Emerg Microbes Infect. 2020;9(1):1467-9.
- Gao X, Wang S, Zeng W, Chen S, Wu J, Lin X, et al. Clinical and immunologic features among COVID-19-affected mother-infant pairs: antibodies to SARS-CoV-2 detected in breast milk. New Microbes New Infect. 2020;37:100752.
- Martins-Filho PR, Tanajura DM, Santos HP, Jr., Santos VS. COVID-19 during pregnancy: Potential risk for neurodevelopmental disorders in neonates? Eur J Obstet Gynecol Reprod Biol. 2020;250:255-6.
- Phelan AL, Katz R, Gostin LO. The Novel Coronavirus Originating in Wuhan, China: Challenges for Global Health Governance. JAMA. 2020.
- Coronaviridae Study Group of the International Committee on Taxonomy of V. The species Severe acute respiratory syndrome-related coronavirus: classifying 2019-nCoV and naming it SARS-CoV-2. Nat Microbiol. 2020;5(4):536-44.
- Gerste RD. Thrombose-Pathogenese: Endotheldysfunktion bei COVID-19. Deutsches Ärzteblatt. 2020;22-23/2020:2.
- Varga Z, Flammer AJ, Steiger P, Haberecker M, Andermatt R, Zinkernagel AS, et al. Endothelial cell infection and endotheliitis in COVID-19. Lancet. 2020;395(10234):1417-8.
- Campbell KH, Tornatore JM, Lawrence KE, Illuzzi JL, Sussman LS, Lipkind HS, et al. Prevalence of SARS-CoV-2 Among Patients Admitted for Childbirth in Southern Connecticut. JAMA. 2020.
- Zöllkau J BM, Scherag A, Schleußner E, Groten T. Periodenprävalenz von SARS-CoV-2 in einer unselektierten Stichprobe schwangerer Frauen in Jena – Thüringen. ZGN2020.
- Mauvais-Jarvis F, Klein SL, Levin ER. Estradiol, Progesterone, Immunomodulation, and COVID-19 Outcomes. Endocrinology. 2020;161(9).
- Pettirosso E, Giles M, Cole S, Rees M. COVID-19 and pregnancy: A review of clinical characteristics, obstetric outcomes and vertical transmission. Aust N Z J Obstet Gynaecol. 2020.
- Stanczyk P, Jachymski T, Sieroszewski P. COVID-19 during pregnancy, delivery and postpartum period based on EBM. Ginekol Pol. 2020;91(7):417-23.
- Selim M, Mohamed S, Abdo M, Abdelhaffez A. Is COVID-19 Similar in Pregnant and Non-Pregnant Women? Cureus. 2020;12(6):e8888.
- Wenling Y, Junchao Q, Xiao Z, Ouyang S. Pregnancy and COVID-19: management and challenges. Rev Inst Med Trop Sao Paulo. 2020;62:e62.
- Thompson JL, Nguyen LM, Noble KN, Aronoff DM. COVID-19-related disease severity in pregnancy. Am J Reprod Immunol. 2020:e13339.
- Hanna N, Hanna M, Sharma S. Is pregnancy an immunological contributor to severe or controlled COVID-19 disease? Am J Reprod Immunol. 2020:e13317.
- Molteni E, Astley CM, Ma W, Sudre CH, Magee LA, Murray B, et al. SARS-CoV-2 (COVID-19) infection in pregnant women: characterization of symptoms and syndromes predictive of disease and severity through real-time, remote participatory epidemiology. medRxiv. 2020.
- Di Mascio D, Sen C, Saccone G, Galindo A, Grunebaum A, Yoshimatsu J, et al. Risk factors associated with adverse fetal outcomes in pregnancies affected by Coronavirus disease 2019 (COVID-19): a secondary analysis of the WAPM study on COVID-19. J Perinat Med. 2020.
- Blitz MJ, Rochelson B, Prasannan L, Shan W, Chervenak FA, Nimaroff M, et al. Race/ethnicity and spatiotemporal trends in SARS-CoV-2 prevalence on obstetrical units in New York. Am J Obstet Gynecol MFM. 2020:100212.
- Emeruwa UN, Spiegelman J, Ona S, Kahe K, Miller RS, Fuchs KM, et al. Influence of Race and Ethnicity on Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2) Infection Rates and Clinical Outcomes in Pregnancy. Obstet Gynecol. 2020.
- Flannery DD, Gouma S, Dhudasia MB, Mukhopadhyay S, Pfeifer MR, Woodford EC, et al. SARS-CoV-2 seroprevalence among parturient women in Philadelphia. Sci Immunol. 2020;5(49).
- Pineles BL, Alamo IC, Farooq N, Green J, Blackwell SC, Sibai BM, et al. Racial-ethnic disparities and pregnancy outcomes in SARS-CoV-2 infection in a universally-tested cohort in Houston, Texas. Eur J Obstet Gynecol Reprod Biol. 2020.
- Metz TD, Collier C, Hollier LM. Maternal Mortality From Coronavirus Disease 2019 (COVID-19) in the United States. Obstet Gynecol. 2020;136(2):313-6.
- Kayem G, Lecarpentier E, Deruelle P, Bretelle F, Azria E, Blanc J, et al. A snapshot of the Covid-19 pandemic among pregnant women in France. J Gynecol Obstet Hum Reprod. 2020;49(7):101826.
- Kucirka LM, Norton A, Sheffield J. Severity of COVID-19 In Pregnancy: A Review of Current Evidence. Am J Reprod Immunol. 2020:e13332.
- Breslin N, Baptiste C, Gyamfi-Bannerman C, Miller R, Martinez R, Bernstein K, et al. COVID-19 infection among asymptomatic and symptomatic pregnant women: Two weeks of confirmed presentations to an affiliated pair of New York City hospitals. Am J Obstet Gynecol MFM. 2020:100118.
- Gao YJ, Ye L, Zhang JS, Yin YX, Liu M, Yu HB, et al. Clinical features and outcomes of pregnant women with COVID-19: a systematic review and meta-analysis. BMC Infect Dis. 2020;20(1):564.
- Antoun L, Taweel NE, Ahmed I, Patni S, Honest H. Maternal COVID-19 infection, clinical characteristics, pregnancy, and neonatal outcome: A prospective cohort study. Eur J Obstet Gynecol Reprod Biol. 2020;252:559-62.
- Ellington S, Strid P, Tong VT, Woodworth K, Galang RR, Zambrano LD, et al. Characteristics of Women of Reproductive Age with Laboratory-Confirmed SARS-CoV-2 Infection by Pregnancy Status – United States, January 22-June 7, 2020. MMWR Morb Mortal Wkly Rep. 2020;69(25):769-75.
- Reis H, Boldrini NAT, Caldas JVJ, Paz A, Ferrugini CLP, Miranda AE. Severe coronavirus infection in pregnancy: challenging cases report. Rev Inst Med Trop Sao Paulo. 2020;62:e49.
- Barbero P, Muguerza L, Herraiz I, Garcia Burguillo A, San Juan R, Forcen L, et al. SARS-CoV-2 in pregnancy: characteristics and outcomes of hospitalized and non-hospitalized women due to COVID-19. J Matern Fetal Neonatal Med. 2020:1-7.
- San-Juan R, Barbero P, Fernandez-Ruiz M, Lopez-Medrano F, Lizasoain M, Hernandez-Jimenez P, et al. Incidence and clinical profiles of COVID-19 pneumonia in pregnant women: A single-centre cohort study from Spain. EClinicalMedicine. 2020;23:100407.
- Allotey J, Stallings E, Bonet M, Yap M, Chatterjee S, Kew T, et al. Clinical manifestations, risk factors, and maternal and perinatal outcomes of coronavirus disease 2019 in pregnancy: living systematic review and meta-analysis. BMJ. 2020;370:m3320.
- Khoury R, Bernstein PS, Debolt C, Stone J, Sutton DM, Simpson LL, et al. Characteristics and Outcomes of 241 Births to Women With Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2) Infection at Five New York City Medical Centers. Obstet Gynecol. 2020;136(2):273-82.
- Cohen J, Vignaux O, Jacquemard F. Covid-19 in pregnant women: General data from a French National Survey. Eur J Obstet Gynecol Reprod Biol. 2020;251:267-8.
- Boyles GP, Thung S, Gabbe SG, Landon MB, Costantine MM. Practical Considerations for Pregnant Women with Diabetes and SARS-CoV-2 Infection. Am J Obstet Gynecol MFM. 2020:100210.
- Boyadzhieva VV, Stoilov NR, Stoilov RM. Coronavirus disease 2019 (COVID-19) during pregnancy in patients with rheumatic diseases. Rheumatol Int. 2020;40(11):1753-62.
- Yam C, Jokubaitis V, Hellwig K, Dobson R. MS, pregnancy and COVID-19. Mult Scler. 2020;26(10):1137-46.
- Khalil A, Kalafat E, Benlioglu C, O’Brien P, Morris E, Draycott T, et al. SARS-CoV-2 infection in pregnancy: A systematic review and meta-analysis of clinical features and pregnancy outcomes. EClinicalMedicine. 2020;25:100446.
- Di Mascio D, COVID Wwgo. Maternal and Perinatal Outcomes of Pregnant Women with SARS-COV-2 infection. Ultrasound Obstet Gynecol. 2020.
- Diriba K, Awulachew E, Getu E. The effect of coronavirus infection (SARS-CoV-2, MERS-CoV, and SARS-CoV) during pregnancy and the possibility of vertical maternal-fetal transmission: a systematic review and meta-analysis. Eur J Med Res. 2020;25(1):39.
- Prochaska E, Jang M, Burd I. COVID-19 in pregnancy: Placental and neonatal involvement. Am J Reprod Immunol. 2020:e13306.
- Oncel MY, Akin IM, Kanburoglu MK, Tayman C, Coskun S, Narter F, et al. A multicenter study on epidemiological and clinical characteristics of 125 newborns born to women infected with COVID-19 by Turkish Neonatal Society. Eur J Pediatr. 2020.
- Panagiotakopoulos L, Myers TR, Gee J, Lipkind HS, Kharbanda EO, Ryan DS, et al. SARS-CoV-2 Infection Among Hospitalized Pregnant Women: Reasons for Admission and Pregnancy Characteristics – Eight U.S. Health Care Centers, March 1-May 30, 2020. MMWR Morb Mortal Wkly Rep. 2020;69(38):1355-9.
- Delahoy MJ, Whitaker M, O’Halloran A, Chai SJ, Kirley PD, Alden N, et al. Characteristics and Maternal and Birth Outcomes of Hospitalized Pregnant Women with Laboratory-Confirmed COVID-19 – COVID-NET, 13 States, March 1-August 22, 2020. MMWR Morb Mortal Wkly Rep. 2020;69(38):1347-54.
- Pirkle CM. Evidence based care for pregnant women with covid-19. BMJ. 2020;370:m3510.
- London V, McLaren R, Jr., Atallah F, Cepeda C, McCalla S, Fisher N, et al. The Relationship between Status at Presentation and Outcomes among Pregnant Women with COVID-19. Am J Perinatol. 2020;37(10):991-4.
- Pastick KA, Nicol MR, Smyth E, Zash R, Boulware DR, Rajasingham R, et al. A Systematic Review of Treatment and Outcomes of Pregnant Women With COVID-19-A Call for Clinical Trials. Open Forum Infect Dis. 2020;7(9):ofaa350.
- Hessami K, Homayoon N, Hashemi A, Vafaei H, Kasraeian M, Asadi N. COVID-19 and maternal, fetal and neonatal mortality: a systematic review. J Matern Fetal Neonatal Med. 2020:1-6.
- Li W, Yu N, Kang Q, Zeng W, Deng D, Chen S, et al. Clinical manifestations and maternal and perinatal outcomes with COVID-19. Am J Reprod Immunol. 2020:e13340.
- Galang RR, Chang K, Strid P, Snead MC, Woodworth KR, House LD, et al. Severe Coronavirus Infections in Pregnancy: A Systematic Review. Obstet Gynecol. 2020;136(2):262-72.
- Longardt AC, Winkler VP, Pecks U. [SARS-CoV-2 and Perinatal Aspects]. Z Geburtshilfe Neonatol. 2020;224(4):181-6.
- Massarotti C, Adriano M, Cagnacci A, Gorlero F, Gustavino C, Vallerino G, et al. Asymptomatic SARS-CoV-2 infections in pregnant patients in an Italian city during the complete lockdown. J Med Virol. 2020.
- Tanacan A, Erol SA, Turgay B, Anuk AT, Secen EI, Yegin GF, et al. The rate of SARS-CoV-2 positivity in asymptomatic pregnant women admitted to hospital for delivery: Experience of a pandemic center in Turkey. Eur J Obstet Gynecol Reprod Biol. 2020;253:31-4.
- Herraiz I, Folgueira D, Villalain C, Forcen L, Delgado R, Galindo A. Universal screening for SARS-CoV-2 before labor admission during Covid-19 pandemic in Madrid. J Perinat Med. 2020.
- Miller ES, Grobman WA, Sakowicz A, Rosati J, Peaceman AM. Clinical Implications of Universal Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2) Testing in Pregnancy. Obstet Gynecol. 2020;136(2):232-4.
- Prabhu M, Cagino K, Matthews KC, Friedlander RL, Glynn SM, Kubiak JM, et al. Pregnancy and postpartum outcomes in a universally tested population for SARS-CoV-2 in New York City: a prospective cohort study. BJOG. 2020.
- Trippella G, Ciarcia M, Ferrari M, Buzzatti C, Maccora I, Azzari C, et al. COVID-19 in Pregnant Women and Neonates: A Systematic Review of the Literature with Quality Assessment of the Studies. Pathogens. 2020;9(6).
- Crovetto F, Crispi F, Llurba E, Figueras F, Gomez-Roig MD, Gratacos E. Seroprevalence and presentation of SARS-CoV-2 in pregnancy. Lancet. 2020;396(10250):530-1.
- Marin Gabriel MA, Reyne Vergeli M, Caserio Carbonero S, Sole L, Carrizosa Molina T, Rivero Calle I, et al. Maternal, Perinatal and Neonatal Outcomes With COVID-19: A Multicenter Study of 242 Pregnancies and Their 248 Infant Newborns During Their First Month of Life. Pediatr Infect Dis J. 2020.
- Spinato G, Fabbris C, Polesel J, Cazzador D, Borsetto D, Hopkins C, et al. Alterations in Smell or Taste in Mildly Symptomatic Outpatients With SARS-CoV-2 Infection. JAMA. 2020.
- Moein ST, Hashemian SM, Mansourafshar B, Khorram-Tousi A, Tabarsi P, Doty RL. Smell dysfunction: a biomarker for COVID-19. Int Forum Allergy Rhinol. 2020.
- Yang H, Sun G, Tang F, Peng M, Gao Y, Peng J, et al. Clinical features and outcomes of pregnant women suspected of coronavirus disease 2019. J Infect. 2020.
- Yan J, Guo J, Fan C, Juan J, Yu X, Li J, et al. Coronavirus disease 2019 in pregnant women: a report based on 116 cases. Am J Obstet Gynecol. 2020;223(1):111 e1- e14.
- Juan J, Gil MM, Rong Z, Zhang Y, Yang H, Poon LC. Effect of coronavirus disease 2019 (COVID-19) on maternal, perinatal and neonatal outcome: systematic review. Ultrasound Obstet Gynecol. 2020;56(1):15-27.
- Hachem R, Markou GA, Veluppillai C, Poncelet C. Late miscarriage as a presenting manifestation of COVID-19. Eur J Obstet Gynecol Reprod Biol. 2020;252:614.
- Mullins E, Evans D, Viner RM, O’Brien P, Morris E. Coronavirus in pregnancy and delivery: rapid review. Ultrasound Obstet Gynecol. 2020;55(5):586-92.
- Kirtsman M, Diambomba Y, Poutanen SM, Malinowski AK, Vlachodimitropoulou E, Parks WT, et al. Probable congenital SARS-CoV-2 infection in a neonate born to a woman with active SARS-CoV-2 infection. CMAJ. 2020;192(24):E647-E50.
- Mulvey JJ, Magro CM, Ma LX, Nuovo GJ, Baergen RN. WITHDRAWN: A mechanistic analysis placental intravascular thrombus formation in COVID-19 patients. Ann Diagn Pathol. 2020;46:151529.
- Smithgall MC, Liu-Jarin X, Hamele-Bena D, Cimic A, Mourad M, Debelenko L, et al. Third-trimester placentas of severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2)-positive women: histomorphology, including viral immunohistochemistry and in-situ hybridization. Histopathology. 2020.
- Sharps MC, Hayes DJL, Lee S, Zou Z, Brady CA, Almoghrabi Y, et al. A structured review of placental morphology and histopathological lesions associated with SARS-CoV-2 infection. Placenta. 2020;101:13-29.
- Gulersen M, Prasannan L, Tam HT, Metz CN, Rochelson B, Meirowitz N, et al. Histopathological evaluation of placentas after diagnosis of maternal SARS-CoV-2 infection. Am J Obstet Gynecol MFM. 2020:100211.
- Ahlberg M, Neovius M, Saltvedt S, Soderling J, Pettersson K, Brandkvist C, et al. Association of SARS-CoV-2 Test Status and Pregnancy Outcomes. JAMA. 2020.
- Zelop CM, Bonney EA. COVID-19 in pregnancy: possible mechanisms not to be discounted. J Matern Fetal Neonatal Med. 2020:1-4.
- Abbas AM, Ahmed OA, Shaltout AS. COVID-19 and maternal pre-eclampsia: A synopsis. Scand J Immunol. 2020;92(3):e12918.
- Zaigham M, Andersson O. Maternal and perinatal outcomes with COVID-19: A systematic review of 108 pregnancies. Acta Obstet Gynecol Scand. 2020.
- Dashraath P, Wong JLJ, Lim MXK, Lim LM, Li S, Biswas A, et al. Coronavirus disease 2019 (COVID-19) pandemic and pregnancy. Am J Obstet Gynecol. 2020.
- Stumpfe FM, Titzmann A, Schneider MO, Stelzl P, Kehl S, Fasching PA, et al. SARS-CoV-2 Infection in Pregnancy – a Review of the Current Literature and Possible Impact on Maternal and Neonatal Outcome. Geburtshilfe Frauenheilkd. 2020;80(4):380-90.
- Khalil A, von Dadelszen P, Draycott T, Ugwumadu A, O’Brien P, Magee L. Change in the Incidence of Stillbirth and Preterm Delivery During the COVID-19 Pandemic. JAMA. 2020.
- Thayer ZM, Gildner TE. COVID-19-related financial stress associated with higher likelihood of depression among pregnant women living in the United States. Am J Hum Biol. 2020:e23508.
- Zhou Y, Shi H, Liu Z, Peng S, Wang R, Qi L, et al. The prevalence of psychiatric symptoms of pregnant and non-pregnant women during the COVID-19 epidemic. Transl Psychiatry. 2020;10(1):319.
- Ayaz R, Hocaoglu M, Gunay T, Yardimci OD, Turgut A, Karateke A. Anxiety and depression symptoms in the same pregnant women before and during the COVID-19 pandemic. J Perinat Med. 2020.
- Farrell T, Reagu S, Mohan S, Elmidany R, Qaddoura F, Ahmed EE, et al. The impact of the COVID-19 pandemic on the perinatal mental health of women. J Perinat Med. 2020.
- Dell’Utri C, Manzoni E, Cipriani S, Spizzico C, Dell’Acqua A, Barbara G, et al. Effects of SARS Cov-2 epidemic on the obstetrical and gynecological emergency service accesses. What happened and what shall we expect now? Eur J Obstet Gynecol Reprod Biol. 2020;254:64-8.
- Meyer R, Levin G, Hendin N, Katorza E. Impact of the COVID-19 Outbreak on Routine Obstetrical Management. Isr Med Assoc J. 2020;8(22):417-22.
- Ahmed S, Zimba O, Gasparyan AY. Thrombosis in Coronavirus disease 2019 (COVID-19) through the prism of Virchow’s triad. Clin Rheumatol. 2020;39(9):2529-43.
- Bivia-Roig G, La Rosa VL, Gomez-Tebar M, Serrano-Raya L, Amer-Cuenca JJ, Caruso S, et al. Analysis of the Impact of the Confinement Resulting from COVID-19 on the Lifestyle and Psychological Wellbeing of Spanish Pregnant Women: An Internet-Based Cross-Sectional Survey. Int J Environ Res Public Health. 2020;17(16).
- Turan O, Hakim A, Dashraath P, Jeslyn WJL, Wright A, Abdul-Kadir R. Clinical characteristics, prognostic factors, and maternal and neonatal outcomes of SARS-CoV-2 infection among hospitalized pregnant women: A systematic review. Int J Gynaecol Obstet. 2020.
- Chan JL, Gregory KD, Smithson SS, Naqvi M, Mamelak AN. Pituitary apoplexy associated with acute COVID-19 infection and pregnancy. Pituitary. 2020.
- Tutiya CT, Siaulys MM, Kondo MM, Miglioli-Galvao L, E CAG, Pinheiro CC, et al. Possible formation of pulmonary microthrombi in the early puerperium of pregnant women critically ill with COVID-19: Two case reports. Case Rep Womens Health. 2020;27:e00237.
- Kinsey KE, Ganz E, Khalil S, Brustman L. Intraoperative coagulopathy during cesarean section as an unsuspected initial presentation of COVID-19: a case report. BMC Pregnancy Childbirth. 2020;20(1):481.
- Blumberg DA, Underwood MA, Hedriana HL, Lakshminrusimha S. Vertical Transmission of SARS-CoV-2: What is the Optimal Definition? Am J Perinatol. 2020;37(8):769-72.
- Wang C, Zhou YH, Yang HX, Poon LC. Intrauterine vertical transmission of SARS-CoV-2: what we know so far. Ultrasound Obstet Gynecol. 2020;55(6):724-5.
- Hou H, Wang T, Zhang B, Luo Y, Mao L, Wang F, et al. Detection of IgM and IgG antibodies in patients with coronavirus disease 2019. Clin Transl Immunology. 2020;9(5):e01136.
- Thomas P, Alexander PE, Ahmed U, Elderhorst E, El-Khechen H, Mammen MJ, et al. Vertical transmission risk of SARS-CoV-2 infection in the third trimester: a systematic scoping review. J Matern Fetal Neonatal Med. 2020:1-8.
- Vivanti AJ, Vauloup-Fellous C, Prevot S, Zupan V, Suffee C, Do Cao J, et al. Transplacental transmission of SARS-CoV-2 infection. Nat Commun. 2020;11(1):3572.
- Elkafrawi D, Joseph J, Schiattarella A, Rodriguez B, Sisti G. Intrauterine transmission of COVID-19 in Pregnancy: case report and review of literature. Acta Biomed. 2020;91(3):e2020041.
- Alzamora MC, Paredes T, Caceres D, Webb CM, Valdez LM, La Rosa M. Severe COVID-19 during Pregnancy and Possible Vertical Transmission. Am J Perinatol. 2020;37(8):861-5.
- Zeng L, Xia S, Yuan W, Yan K, Xiao F, Shao J, et al. Neonatal Early-Onset Infection With SARS-CoV-2 in 33 Neonates Born to Mothers With COVID-19 in Wuhan, China. JAMA Pediatr. 2020;174(7):722-5.
- Sagheb S, Lamsehchi A, Jafary M, Atef-Yekta R, Sadeghi K. Two seriously ill neonates born to mothers with COVID-19 pneumonia- a case report. Ital J Pediatr. 2020;46(1):137.
- Kotlyar AM, Grechukhina O, Chen A, Popkhadze S, Grimshaw A, Tal O, et al. Vertical transmission of coronavirus disease 2019: a systematic review and meta-analysis. Am J Obstet Gynecol. 2020.
- Rubio Lorente AM, Pola Guillen M, Lopez Jimenez N, Moreno-Cid Garcia-Suelto M, Rodriguez Rodriguez E, Pascual Pedreno A. Study of amniotic fluid in pregnant women infected with SARS-CoV-2 in first and second trimester. Is there evidence of vertical transmission? J Matern Fetal Neonatal Med. 2020:1-3.
- Mongula JE, Frenken MWE, van Lijnschoten G, Arents NLA, de Wit-Zuurendonk LD, Schimmel-de Kok APA, et al. COVID-19 during pregnancy: non-reassuring fetal heart rate, placental pathology and coagulopathy. Ultrasound Obstet Gynecol. 2020.
- Dong L, Tian J, He S, Zhu C, Wang J, Liu C, et al. Possible Vertical Transmission of SARS-CoV-2 From an Infected Mother to Her Newborn. JAMA. 2020.
- Zeng H, Xu C, Fan J, Tang Y, Deng Q, Zhang W, et al. Antibodies in Infants Born to Mothers With COVID-19 Pneumonia. JAMA. 2020.
- Wang W, Xu Y, Gao R, Lu R, Han K, Wu G, et al. Detection of SARS-CoV-2 in Different Types of Clinical Specimens. JAMA. 2020.
- Baud D, Greub G, Favre G, Gengler C, Jaton K, Dubruc E, et al. Second-Trimester Miscarriage in a Pregnant Woman With SARS-CoV-2 Infection. JAMA. 2020.
- Patane L, Morotti D, Giunta MR, Sigismondi C, Piccoli MG, Frigerio L, et al. Vertical transmission of COVID-19: SARS-CoV-2 RNA on the fetal side of the placenta in pregnancies with COVID-19 positive mothers and neonates at birth. Am J Obstet Gynecol MFM. 2020:100145.
- Hecht JL, Quade B, Deshpande V, Mino-Kenudson M, Ting DT, Desai N, et al. SARS-CoV-2 can infect the placenta and is not associated with specific placental histopathology: a series of 19 placentas from COVID-19-positive mothers. Mod Pathol. 2020.
- Cui D, Liu Y, Jiang X, Ding C, Poon LC, Wang H, et al. Single-cell RNA expression profiling of ACE2 and TMPRSS2 in the human trophectoderm and placenta. Ultrasound Obstet Gynecol. 2020.
- Bloise E, Zhang J, Nakpu J, Hamada H, Dunk CE, Li S, et al. Expression of severe acute respiratory syndrome coronavirus 2 cell entry genes, angiotensin-converting enzyme 2 and transmembrane protease serine 2, in the placenta across gestation and at the maternal-fetal interface in pregnancies complicated by preterm birth or preeclampsia. Am J Obstet Gynecol. 2020.
- Faure-Bardon V, Isnard P, Roux N, Leruez-Ville M, Molina T, Bessieres B, et al. Anatomical and timely assessment of protein expression of angiotensin-converting enzyme 2, SARS-CoV-2 specific receptor, in fetal and placental tissues: new insight for perinatal counseling. Ultrasound Obstet Gynecol. 2020.
- Weatherbee BAT, Glover DM, Zernicka-Goetz M. Expression of SARS-CoV-2 receptor ACE2 and the protease TMPRSS2 suggests susceptibility of the human embryo in the first trimester. Open Biol. 2020;10(8):200162.
- Taglauer E, Benarroch Y, Rop K, Barnett E, Sabharwal V, Yarrington C, et al. Consistent localization of SARS-CoV-2 spike glycoprotein and ACE2 over TMPRSS2 predominance in placental villi of 15 COVID-19 positive maternal-fetal dyads. Placenta. 2020;100:69-74.
- Pique-Regi R, Romero R, Tarca AL, Luca F, Xu Y, Alazizi A, et al. Does the human placenta express the canonical cell entry mediators for SARS-CoV-2? Elife. 2020;9.
- Komine-Aizawa S, Takada K, Hayakawa S. Placental barrier against COVID-19. Placenta. 2020;99:45-9.
- Kreis NN, Ritter A, Louwen F, Yuan J. A Message from the Human Placenta: Structural and Immunomodulatory Defense against SARS-CoV-2. Cells. 2020;9(8).
- Hijona Elosegui JJ, Carballo Garcia AL, Fernandez Risquez AC, Bermudez Quintana M, Exposito Montes JF. Does the maternal-fetal transmission of SARS-CoV-2 occur during pregnancy? Rev Clin Esp. 2020.
- Auriti C, De Rose DU, Tzialla C, Caforio L, Ciccia M, Manzoni P, et al. Vertical Transmission of SARS-CoV-2 (COVID-19): Are Hypotheses More than Evidences? Am J Perinatol. 2020;37(S 02):S31-S8.
- Pulinx B, Kieffer D, Michiels I, Petermans S, Strybol D, Delvaux S, et al. Vertical transmission of SARS-CoV-2 infection and preterm birth. Eur J Clin Microbiol Infect Dis. 2020.
- Sisman J, Jaleel MA, Moreno W, Rajaram V, Collins RRJ, Savani RC, et al. Intrauterine Transmission of SARS-COV-2 Infection in a Preterm Infant. Pediatr Infect Dis J. 2020;39(9):e265-e7.
- Deniz M, Tezer H. Vertical transmission of SARS CoV-2: a systematic review. J Matern Fetal Neonatal Med. 2020:1-8.
- Walker KF, O’Donoghue K, Grace N, Dorling J, Comeau JL, Li W, et al. Maternal transmission of SARS-COV-2 to the neonate, and possible routes for such transmission: a systematic review and critical analysis. BJOG. 2020;127(11):1324-36.
- Hayakawa S, Komine-Aizawa S, Mor GG. Covid-19 pandemic and pregnancy. J Obstet Gynaecol Res. 2020.
- Ai T, Yang Z, Hou H, Zhan C, Chen C, Lv W, et al. Correlation of Chest CT and RT-PCR Testing for Coronavirus Disease 2019 (COVID-19) in China: A Report of 1014 Cases. Radiology. 2020;296(2):E32-E40.
- Alay I, Yildiz S, Kaya C, Yasar KK, Aydin OA, Karaosmanoglu HK, et al. The clinical findings and outcomes of symptomatic pregnant women diagnosed with or suspected of having coronavirus disease 2019 in a tertiary pandemic hospital in Istanbul, Turkey. J Obstet Gynaecol Res. 2020.
- Francis S, Mathew RP, Khalid ZA. Coronavirus (COVID-19) Infection in Pregnancy: Does Non-contrast Chest Computed Tomography (CT) Have a Role in Its Evaluation and Management? J Obstet Gynaecol India. 2020;70(4):272-4.
- Yassa M, Yirmibes C, Cavusoglu G, Eksi H, Dogu C, Usta C, et al. Outcomes of universal SARS-CoV-2 testing program in pregnant women admitted to hospital and the adjuvant role of lung ultrasound in screening: a prospective cohort study. J Matern Fetal Neonatal Med. 2020;33(22):3820-6.
- Sperandeo M, Trovato GM. Care of future mothers amid the COVID-19 outbreak: is there a monitoring role for lung ultrasound? Ultrasound Obstet Gynecol. 2020;56(3):469-70.
- Quarato CMI, Venuti M, Lacedonia D, Simeone A, Sperandeo M. Diagnosis and monitoring of COVID-19 pneumonia in pregnant women: is lung ultrasound appropriate? Ultrasound Obstet Gynecol. 2020;56(3):467-8.
- Duffy CR, Hart JM, Modest AM, Hacker MR, Golen T, Li Y, et al. Lymphopenia and Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2) Infection Among Hospitalized Obstetric Patients. Obstet Gynecol. 2020;136(2):229-31.
- Wei L, Gao X, Chen S, Zeng W, Wu J, Lin X, et al. Clinical Characteristics and Outcomes of Childbearing-Age Women With COVID-19 in Wuhan: Retrospective, Single-Center Study. J Med Internet Res. 2020;22(8):e19642.
- Vivanti AJ, Mattern J, Vauloup-Fellous C, Jani J, Rigonnot L, El Hachem L, et al. Retrospective Description of Pregnant Women Infected with Severe Acute Respiratory Syndrome Coronavirus 2, France. Emerg Infect Dis. 2020;26(9):2069-76.
- Vlachodimitropoulou Koumoutsea E, Vivanti AJ, Shehata N, Benachi A, Le Gouez A, Desconclois C, et al. COVID-19 and acute coagulopathy in pregnancy. J Thromb Haemost. 2020;18(7):1648-52.
- Federici L, Picone O, Dreyfuss D, Sibiude J. Successful continuation of pregnancy in a patient with COVID-19-related ARDS. BMJ Case Rep. 2020;13(8).
- Futterman I, Toaff M, Navi L, Clare CA. COVID-19 and HELLP: Overlapping Clinical Pictures in Two Gravid Patients. AJP Rep. 2020;10(2):e179-e82.
- Zitiello A, Grant GE, Ben Ali N, Feki A. Thrombocytopaenia in pregnancy: the importance of differential diagnosis during the COVID-19 pandemic. J Matern Fetal Neonatal Med. 2020:1-3.
- Ahmed I, Eltaweel N, Antoun L, Rehal A. Severe pre-eclampsia complicated by acute fatty liver disease of pregnancy, HELLP syndrome and acute kidney injury following SARS-CoV-2 infection. BMJ Case Rep. 2020;13(8).
- Avila WS, Carvalho RC. COVID-19: A New Challenge in Pregnancy and Heart Disease. Arq Bras Cardiol. 2020;115(1):1-4.
- Dap M, Morel O. Proteinuria in Covid-19 pregnant women: Preeclampsia or severe infection? Eur J Obstet Gynecol Reprod Biol. 2020;252:612.
- Louchet M, Sibiude J, Peytavin G, Picone O, Treluyer JM, Mandelbrot L. Placental transfer and safety in pregnancy of medications under investigation to treat coronavirus disease 2019. Am J Obstet Gynecol MFM. 2020;2(3):100159.
- Maldarelli GA, Savage M, Mazur S, Oxford-Horrey C, Salvatore M, Marks KM. Remdesivir Treatment for Severe COVID-19 in Third-Trimester Pregnancy: Case Report and Management Discussion. Open Forum Infect Dis. 2020;7(9):ofaa345.
- Mulangu S, Dodd LE, Davey RT, Jr., Tshiani Mbaya O, Proschan M, Mukadi D, et al. A Randomized, Controlled Trial of Ebola Virus Disease Therapeutics. N Engl J Med. 2019;381(24):2293-303.
- Wang Y, Zhang D, Du G, Du R, Zhao J, Jin Y, et al. Remdesivir in adults with severe COVID-19: a randomised, double-blind, placebo-controlled, multicentre trial. Lancet. 2020;395(10236):1569-78.
- Lacroix I, Benevent J, Damase-Michel C. Chloroquine and hydroxychloroquine during pregnancy: What do we know? Therapie. 2020;75(4):384-5.
- Huybrechts KF, Bateman BT, Zhu Y, Straub L, Mogun H, Kim SC, et al. Hydroxychloroquine early in Pregnancy and Risk of Birth Defects. Am J Obstet Gynecol. 2020.
- Oxford Uo. RECOVERY trial, interim results 2020 [Available from: https://www.recoverytrial.net/results.
- Government U. World’s first coronavirus treatment approved for NHS use by Government 2020 [Available from: https://www.gov.uk/government/news/world-first-coronavirus-treatment-approved-for-nhs-use-by-government approved-for-nhs-use-by-government.
- Trials C. Randomised Evaluation of COVID-19 Therapy (RECOVERY) 2020 [Available from: https://clinicaltrials.gov/ct2/show/NCT04381936
- Gavillet M, Rolnik DL, Hoffman MK, Panchaud A, Baud D. Should we stop aspirin prophylaxis in pregnant women diagnosed with COVID-19? Ultrasound Obstet Gynecol. 2020;55(6):843-4.







